Tłumaczyła lek. Iwona Rywczak
Konsultowała prof. dr hab. n. med. Przemysława Jarosz-Chobot, Klinika Diabetologii Dziecięcej
Śląskiego Uniwersytetu Medycznego w Katowicach
Skróty: ACE – inhibitory konwertazy angiotensyny, ADA – American Diabetes Association, BMI – wskaźnik masy ciała, GLP-1 – agoniści receptora peptydu glukagonopodobnego, IFG – nieprawidłowa glikemia na czczo, IGT – upośledzona tolerancja glukozy, NAFLD – niealkoholowa choroba stłuszczeniowa wątroby, OGTT – test doustnego obciążenia glukozą, PCOS – zespół wielotorbielowatych jajników, SMBG – samokontrola glikemii, TZD – pochodne tiazolidynodionu
Podsumowanie i zalecenia
Badania przesiewowe w kierunku cukrzycy typu 2 u młodzieży z grupy ryzyka
· Nierozpoznana cukrzyca typu 2 występuje bardzo rzadko u nastolatków (A).
· Powszechne wykonywanie badań przesiewowych u otyłych nastolatków prawdopodobnie nie jest efektywne
kosztowo w większości populacji (E).
– Przesiewowe oznaczanie glukozy w moczu u nastoletnich
Japończyków może być pojedynczym
przypadkiem, w którym udowodniono efektywność
kosztową.
· Badania w kierunku nieprawidłowej glikemii u otyłych nastolatków z grupy ryzyka należy przeprowadzać w ramach oceny klinicznej chorób współistniejących związanych z otyłością (niealkoholowa choroba stłuszczeniowa wątroby [NAFLD], hipertriglicerydemia, podwyższone ciśnienie tętnicze), które występują częściej niż nieprawidłowa glikemia (E).
Rozpoznanie i ustalenie typu cukrzycy
· Cukrzycę typu 2 należy rozpoznawać zgodnie z kryteriami American Diabetes Association (ADA). (E)
– Rozpoznanie można oprzeć na oznaczeniu glikemii
na czczo, 2 h po obciążeniu glukozą lub oznaczeniu
odsetka hemoglobiny A1c (HbA1c).
– Przy braku objawów cukrzycy badania należy powtórzyć w innym dniu.
– Lekarze powinni być świadomi, że każdy z powyższych
testów ma pewne ograniczenia.
· Oznaczenie autoprzeciwciał związanych z cukrzycą
należy rozważyć u wszystkich dzieci, u których ustalono
kliniczne rozpoznanie cukrzycy typu 2 ze względu
na częste występowanie autoimmunizacji obejmującej
wyspy trzustkowe u pacjentów z poza tym „typowymi”
objawami cukrzycy typu 2 (E).
– Dzieci przed okresem pokwitania praktycznie nie
chorują na cukrzycę typu 2, nawet jeśli występuje u nich otyłość (A).
– Obecność autoprzeciwciał wskazuje na typ 1 cukrzycy i konieczność szybszego rozpoczęcia leczenia
insuliną (A).
– Występowanie autoprzeciwciał wskazuje na konieczność
uwzględnienia obecności innych zaburzeń o podłożu autoimmunizacyjnym (A).
· Oznaczenie autoprzeciwciał związanych z cukrzycą należy rozważyć u dzieci w okresie dojrzewania z nadwagą lub otyłością oraz objawami klinicznymi cukrzycy typu 1 (A).
· Ocenę w kierunku klinicznie istotnych powikłań i chorób współistniejących związanych z cukrzycą należy przeprowadzić w momencie rozpoznania cukrzycy (A).
– Rozpoznając cukrzycę, należy oznaczyć stężenie
triglicerydów i aktywność enzymów wątrobowych w celu wykluczenia ostrych zaburzeń istotnych klinicznie
(E).
– W momencie rozpoznania cukrzycy należy oznaczyć
wskaźnik albumina/kreatynina.
– W momencie rozpoznania cukrzycy pacjentów należy
ocenić pod kątem obturacyjnego bezdechu
podczas snu, ciąży i depresji (E).
Leczenie wstępne
· Modyfikację stylu życia należy rozpocząć w momencie rozpoznania cukrzycy typu 2 (E).
· W leczeniu wstępnym cukrzycy typu 2 u młodzieży należy zastosować metforminę i/lub insulinę w monoterapii lub terapii skojarzonej (A).
· Leczenie wstępne zależy od objawów, stopnia ciężkości
hiperglikemii oraz obecności lub braku ketozy/
kwasicy ketonowej (E).
– W przypadku obecności objawów klinicznych, możliwe
jest gwałtowne pogorszenie stanu chorego
niezależnie od ostatecznej klasyfikacji choroby, dlatego
konieczna jest szybka diagnostyka i wdrożenie
odpowiedniego leczenia (E).
– U chorych stabilnych metabolicznie (HbA1c<9, brak
objawów) leczenie należy rozpocząć od podania
metforminy w monoterapii (A).
(i) Dawka początkowa wynosi 500 mg/24 h przez 7 dni. Dawkę należy zwiększać raz w tygodniu o 500 mg w ciągu 3–4 tygodni aż do uzyskania
dawki maksymalnej wynoszącej 1000 mg 2 razy/24 h (można zastosować preparat o przedłużonym
uwalnianiu, jeśli jest dostępny).
– U chorych niestabilnych metabolicznie konieczne
jest zastosowanie insuliny (A).
(i) Kontrolę metaboliczną często można przywrócić,
podając raz/24 h insulinę NPH lub podstawową
(dawka początkowa 0,25–0,5 j./kg mc.).
(ii) Równocześnie można wprowadzić metforminę,
jeżeli u chorego nie stwierdza się kwasicy.
(iii) Leczenie insuliną zwykle można zmienić na leczenie
metforminą w monoterapii po 2–6 tygodniach.
· Celem wstępnego leczenia powinno być uzyskanie wartości HbA1c <6,5% (B).
· Należy regularnie samokontrolować glikemię (SMBG). Częstotliwość monitorowania jest osobnicza i zależy od stopnia kontroli glikemii oraz dostępnych środków (E).
Leczenie w późniejszym etapie choroby
· Jeśli w ciągu 3–4 miesięcy leczenia wyłącznie metforminą nie uda się uzyskać docelowego odsetka HbA1c <6,5%, należy silnie rozważyć dodanie insuliny podstawowej (A).
· Jeśli nie uda się uzyskać takiego poziomu HbA1c w trakcie leczenia skojarzonego metforminą i insuliną podstawową (w dawce do 1,2 j./kg mc.), należy dołączyć bolus posiłkowy insuliny, a następnie modyfikować jego dawkę do momentu uzyskania wartości <6,5% (B).
· Preparaty z innych grup oceniono w pojedynczych badaniach i większość z nich nie jest zarejestrowana do stosowania u młodzieży (E).
Rozpoznawanie i leczenie chorób współistniejących oraz powikłań
· Wskaźnik albumina/kreatynina należy oznaczyć przy
ustalaniu rozpoznania cukrzycy, a następnie powtarzać
co roku (A):
(i) Zwiększenie wskaźnika albumina/kreatynina w moczu
należy potwierdzić w 2 z 3 próbek.
– W przypadku potwierdzenia zwiększenia wskaźnika
albumina/kreatynina w moczu należy rozpocząć
leczenie inhibitorem konwertazy angiotensyny
(ACE), modyfikując dawkę leku co 3 miesiące aż
do unormowania wskaźnika (A).
· Ciśnienie tętnicze krwi należy mierzyć na każdej wizycie
zgodnie ze standaryzowanymi metodami przeznaczonymi
dla dzieci (A).
(i) Podwyższenie ciśnienia tętniczego należy potwierdzić w dwóch dodatkowych pomiarach przeprowadzonych w różnych dniach.
(ii) Nadciśnienie tętnicze definiuje się jako średnie
skurczowe lub rozkurczowe ciśnienie tętnicze
>95. centyla dla wieku, płci i wzrostu. Wysokie
prawidłowe ciśnienie tętnicze mieści się w zakresie
od 90. do <95. centyla.
– Wstępne leczenie powinno polegać na zmniejszeniu
masy ciała, ograniczeniu soli w diecie i zwiększeniu
aktywności fizycznej (E).
– Jeżeli po 6 miesiącach wartości ciśnienia tętniczego
przekraczają 95. centyl, należy rozpocząć leczenie
ACE, a dawkę należy modyfikować do uzyskania
wartości <90. centyla (A).
(i) W przypadku nietolerancji ACE z powodu działań
niepożądanych można zastosować antagonistę
receptora angiotensyny, antagonistę kanału wapniowego
lub diuretyk (E).
(ii) Jeżeli ciśnienie tętnicze nie ulegnie normalizacji w trakcie stosowania jednego leku, konieczne
może być leczenie skojarzone (E).
Badanie w kierunku dyslipidemii należy przeprowadzić
wkrótce po ustaleniu rozpoznania, gdy osiągnie się
prawidłową kontrolę glikemii, a następnie powtarzać
co roku (A).
– Cholesterol
(i) Wartości docelowe:
cholesterol frakcji LDL (lipoproteiny o małej gęstości)
<100 mg/dl (2,6 mmol/l)
cholesterol frakcji HDL (lipoproteiny o dużej gęstości)
>35 mg/dl (0,91 mmol/l)
triglicerydy <150 mg/dl (1,7 mmol/l)
(ii) Jeżeli stężenie cholesterolu LDL przekracza wartość
docelową, należy zoptymalizować kontrolę
glikemii i zalecić dietę zgodnie z wytycznymi AHA
(dieta II etapu).
Kolejną kontrolę profilu lipidowego na czczo należy
przeprowadzić za 6 miesięcy.
(iii) Jeżeli stężenie cholesterolu LDL nadal przekracza
130 mg/dl, należy rozpocząć leczenie farmakologiczne.
Jako wartość docelową należy przyjąć
stężenie <130 mg/dl, optymalnie <100 mg/dl (E).
(iv) Wykazano, że statyny są bezpiecznymi i skutecznymi
lekami (A).
– Triglicerydy
(i) Jeżeli stężenie triglicerydów wynosi >400 mg/dl
na czczo lub >1000 mg/dl w oznaczeniu przygodnym,
należy rozpocząć leczenie farmakologiczne,
przyjmując jako wartość docelową <400 mg/dl
na czczo (w celu zmniejszenia ryzyka zapalenia
trzustki) (E).
(ii) Lekami z wyboru w terapii hipertriglicerydemii są
fibraty. Wykazano, że są one skuteczne i bezpieczne
(A).
Badanie w kierunku retinopatii należy przeprowadzić w momencie rozpoznania cukrzycy, a następnie powtarzać
je co roku (A).
· Ocenę w kierunku NAFLD należy przeprowadzić w momencie rozpoznania cukrzycy, a następnie powtarzać
ją co roku (A).
– Jeżeli aktywność enzymów wątrobowych jest nadal
zwiększona mimo zmniejszenia masy ciała i uzyskania
kontroli glikemii, chorego należy skierować
do gastroenterologa (E).
· Chorych należy kontrolować pod kątem zaburzeń miesiączkowania, hiperandrogenizmu, depresji oraz obturacyjnego bezdechu podczas snu w momencie rozpoznania cukrzycy, a następnie w regularnych odstępach (E).
· Chorych należy kontrolować pod kątem palenia tytoniu i picia alkoholu w momencie rozpoznania cukrzycy, a następnie w regularnych odstępach (E).
Wprowadzenie
Cukrzyca typu 2 u dzieci i młodzieży staje się coraz ważniejszym problemem zdrowia publicznego na całym świecie,1-17 w wielu krajach ma ona swoistą charakterystykę i dotyczy konkretnych populacji. Ponieważ problem w tej grupie wiekowej jest względnie nowy, istnieją swoiste trudności w rozpoznaniu, leczeniu i monitorowaniu choroby wynikające z niewystarczających danych na temat cukrzycy typu 2 w tej populacji. Brak danych dodatkowo komplikują różnice pomiędzy krajami rozwijającymi się a krajami rozwiniętymi w zakresie charakterystyki i manifestacji choroby oraz metod leczenia. W 2009 roku powstały wytyczne ISPAD dotyczące diagnostyki i leczenia cukrzycy typu 2 u dzieci i młodzieży.18 Od czasu publikacji tych wytycznych zaplanowano i ukończono wiele ważnych badań, dzięki którym dysponujemy istotnie szerszą wiedzą o cukrzycy typu 2. W niniejszym rozdziale omówiono diagnostykę cukrzycy typu 2, jej pierwsze objawy, klasyfikację, leczenie wstępne i w późniejszym okresie choroby, a także monitorowanie oraz leczenie chorób współistniejących i powikłań.
Definicja, klasyfikacja i charakterystyka cukrzycy typu 2 w wieku młodzieńczym
Cukrzyca typu 2 występuje, gdy wydzielanie insuliny nie pokrywa zwiększonego zapotrzebowania spowodowanego insulinoopornością, co prowadzi do względnego niedoboru insuliny.19 Na ogół towarzyszą jej inne zaburzenia metaboliczne typowe dla insulinooporności (dyslipidemia, nadciśnienie tętnicze, zespół wielotorbielowatych jajników [PCOS], stłuszczenie wątroby).20 W przeciwieństwie do cukrzycy typu 1, nie zidentyfikowano żadnego procesu autoimmunizacyjnego prowadzącego do niedostatecznego wydzielania insuliny w cukrzycy typu 2,20 a przyczyną niewystarczającego wydzielania insuliny wydają się być czynniki genetyczne, środowiskowe i metaboliczne, które mogą być różne u poszczególnych pacjentów. Wydzielanie insuliny jest zależne od stadium oraz czasu trwania choroby i może być zróżnicowane od opóźnionego, ale wyraźnie zwiększonego w odpowiedzi na obciążenie glukozą, do bezwzględnie zmniejszonego.19 U dorosłych z objawami klinicznymi w momencie rozpoznania wydzielanie insuliny jest zmniejszone o 50%, co może doprowadzić do insulinozależności w ciągu kilku lat.21 Nowe dane pochodzące z badania TODAY (Treatment Options for T2DM in Adolescents and Youth) sugerują, że utrata zdolności wydzielania insuliny zachodzi nawet jeszcze szybciej, gdy cukrzyca typu 2 objawia się w wieku młodzieńczym.22,23 Rozpoznanie cukrzycy typu 2 wymaga dwóch kroków: potwierdzenia obecności cukrzycy, a następnie ustalenia typu choroby. Kryteria i klasyfikację cukrzycy omówiono dokładnie w rozdziale pt. „Definicja, epidemiologia i klasyfikacja cukrzycy u dzieci i młodzieży”.24 Kryteria diagnostyczne cukrzycy opierają się na pomiarach glikemii i występowaniu objawów.25 Istnieją cztery sposoby rozpoznania cukrzycy, a w każdym przypadku, w którym hiperglikemia nie jest jednoznaczna, konieczne jest potwierdzenie rozpoznania w kolejnym dniu za pomocą jednej z czterech metod opisanych poniżej.
Cukrzycę należy rozpoznać, gdy:
• stężenie glukozy w osoczu na czczo (FPG) wynosi
≥7,0 mmol/l (126 mg/dl)
• stężenie glukozy w osoczu po obciążeniu wynosi
>11,1 mmol/l (200 mg/dl) – 1,75 g/kg mc.
(maks. 75 g) bezwodnej glukozy rozpuszczonej w wodzie
• obecne są objawy cukrzycy i glikemia przygodna
wynosi ≥200 mg/dl (11,1 mmol/l).
– Glikemia przygodna oznacza wynik badania
wykonanego o dowolnej porze dnia bez względu
na czas, jaki upłynął od ostatniego posiłku.
– Do objawów cukrzycy zalicza się wielomocz,
wzmożone pragnienie, oddawanie moczu w nocy i niewyjaśnione zmniejszenie masy ciała.
• HbA1c>6,5%
– Oznaczenie należy wykonać w laboratorium
stosującym testy z certyfikatem National Glycohemoglobin
Standardization Program, standaryzowane
zgodnie z DCCT.
• W przypadku braku objawów hiperglikemia
wykryta przypadkowo lub w warunkach ostrego
fizjologicznego stresu może być przejściowa i nie należy jej traktować jako potwierdzenia
rozpoznania cukrzycy
• Na podstawie wyników badań wysunięto wątpliwości
na temat powtarzalności testu doustnego
obciążenia glukozą (OGTT) u otyłych nastolatków
– przy powtórzeniu OGTT w odstępie
kilku tygodni współczynnik zgodności wyniósł
około 30%.26
• Chociaż poziom HbA1c jest uznanym przez ADA
kryterium rozpoznania cukrzycy u dorosłych,
budzi ono kontrowersje, ponieważ identyfikuje
populacje, które nie są do końca zgodne z populacjami
wychwyconymi na podstawie kryterium
stężenia glukozy na czczo lub stężenia po obciążeniu
glukozą.27 Jednak wartość HbA1c>6,5%
wskazuje na ryzyko rozwoju retinopatii podobnie
jak kryteria oparte na stężeniu glukozy. U dzieci nie ustalono zasad stosowania kryterium
HbA1c, dlatego rozpoznając cukrzycę wyłącznie
na podstawie wartości HbA1c, należy
zachować ostrożność.
Po ustaleniu rozpoznania cukrzycy należy rozważyć oznaczenie autoprzeciwciał związanych z cukrzycą u wszystkich dzieci z klinicznym rozpoznaniem cukrzycy typu 2. Wynika to z częstego występowania autoimmunizacji obejmującej wyspy trzustki u pacjentów z poza tym „typową” klinicznie określoną cukrzycą typu 2. Badania wykazały, że w zależności od rasy i grupy etnicznej autoprzeciwciała wykrywa się u 10–20% osób z klinicznie rozpoznaną cukrzycą typu 2.21, 28-32 Obecność przeciwciał wskazuje na szybką progresję do insulinozależności,33 a także na ryzyko wystąpienia innych chorób autoimmunizacyjnych. Oznaczenie autoprzeciwciał związanych z cukrzycą należy również rozważyć u dzieci w okresie dojrzewania z nadwagą lub otyłością, u których obecne są objawy kliniczne cukrzycy typu 1 (utrata masy ciała, ketoza/kwasica ketonowa). Niektóre z nich mogą chorować na cukrzycę typu 2 i przez dłuższy czas mogą nie wymagać leczenia insuliną jeśli choroba jest dobrze kontrolowana.34
Charakterystyka chorych na cukrzycę typu 2 objawiającą się w wieku młodzieńczym
• Choroba występuje najczęściej w drugiej dekadzie
życia, a mediana wieku w chwili rozpoznania
wynosi 13,5 roku. Ten okres współistnieje
ze szczytem fizjologicznej insulinooporności
podczas pokwitania, która może powodować
wystąpienie objawów cukrzycy u nastolatków, u których dotychczas metabolizm glukozy pozostawał w fazie wyrównania. Zgodnie z tym mediana
wieku ujawnienia się cukrzycy u dziewcząt
jest o 1 rok większa niż u chłopców.8,35
• Choroba rzadko objawia się przed pokwitaniem.
8,35
• Krewni pierwszego i drugiego stopnia dzieci
chorych na cukrzycę typu 2 często choruja naten
typ cukrzycy.35,36
• Cukrzyca typu 2 występuje u osób wszystkich
ras, ale ze znaczną przewagą u niewywodzących
się z populacji rasy białej pochodzenia
europejskiego, na przykład Afrykanów, rdzennych
mieszkańców Ameryki Północnej (Indian),
Latynoamerykanów (zwłaszcza Meksykanów),
osób pochodzenia azjatyckiego lub południowoazjatyckiego
(Półwysep Indyjski) oraz rdzennych
mieszkańców wysp Pacyfiku. W badaniu
populacyjnym The SEARCH for Diabetes in
Youth stwierdzono, że odsetek zamieszkujących w Stanach Zjednoczonych osób w wieku
10–19 lat z rozpoznaną cukrzycą typu 2 wykazywał
znaczne różnice zależnie od przynależności
do grup etnicznych: 6% u osób rasy białej
niebędących Latynosami, 22% u Latynosów,
33% u osób rasy czarnej, 40% u osób pochodzenia
azjatyckiego z wysp Pacyfiku i 76% u rdzennych
Amerykanów (Indian).8
• W Hong Kongu 90% przypadków cukrzycy objawiającej
się w wieku młodzieńczym to cukrzyca
typu 2,10 na Tajwanie – 50%,11 a w Japonii niemal
60% przypadków.
• W Stanach Zjednoczonych i w Europie niemal
cała populacja młodzieży chorej na cukrzycę
typu 2 wykazuje wskaźnik masy ciała (BMI)
powyżej 85. centyla dla wieku i płci.35 Takiego
zjawiska nie obserwuje się jednak w krajach
azjatyckich. Otyłości nie stwierdza się u 15% japońskich
dzieci chorych na cukrzycę typu 2.17,37 U połowy dzieci hinduskich chorych na cukrzycę
typu 2, mieszkających w miastach, masa ciała
była prawidłowa (<120% masy ciała należnej
do wzrostu),12 a na Tajwanie połowa dzieci chorych
na cukrzycę typu 2 nie była otyła.11
• Stosunek płci w populacji chorych (chłopcy:
dziewczęta) waha się od 1:4 do 1:6 u rdzennych
mieszkańców Ameryki Północnej (Indian)
do 1:1 u Azjatów i Arabów pochodzących z Libii.
• W Stanach Zjednoczonych i Europie cukrzyca
typu 2 w wieku młodzieńczym na ogół
występuje w populacjach o niskim statusie
społeczno-ekonomicznym i niskim poziomie
wykształcenia,35 natomiast w krajach szybko
rozwijających się, takich jak Chiny i Indie, bardziej
prawdopodobne jest wystąpienie cukrzycy
typu 2 u dzieci z zamożniejszych rodzin niż z biedniejszych.
• Manifestacja cukrzycy typu 2 w wieku młodzieńczym
jest różna – od bezobjawowej hiperglikemii
wykrytej w trakcie badań przesiewowych
lub rutynowych badań lekarskich
do kwasicy ketonowej obserwowanej nawet u 25% chorych38 lub stanu hiperglikemiczno-hiperosmolalnego.
39 Nierozpoznane i nieleczone
dwa ostatnie stany mogą się wiązać z dużym
ryzykiem powikłań i umieralności.
Autoimmunizacja w cukrzycy typu 2
Niektórzy autorzy opisywali zjawisko autoimmunizacyjnej
cukrzycy typu 2. Niekiedy określa się
je jako T1.5, T3 lub podwójna cukrzyca. Jednak
obecnie stało się bardziej jasne, że osoby te należy
traktować jak chorych na autoimmunizacyjną cukrzycę
typu 1 objawiającą się u osób z otyłością lub
nadwagą, ze współistniejącą insulinoopornością.
• U nastolatków i dorosłych w Stanach Zjednoczonych i Europie, u których na podstawie objawów
klinicznych rozpoznano cukrzycę typu 2, w 15–40% przypadków stwierdzano obecność
autoprzeciwciał związanych z cukrzycą typu 1. W tej grupie znajdowało się wiele osób, które nie
otrzymywały insuliny w ciągu roku po ustaleniu
rozpoznania.28-31
• U młodzieży z fenotypem cukrzycy typu 2 z obecnymi
przeciwciałami obserwuje się znamiennie
mniejszą nadwagę, niższe ciśnienie tętnicze,
mniejsze stężenie triglicerydów i większe stężenie
cholesterolu HDL niż u pacjentów nieposiadających
przeciwciał. Dodatkowo obserwuje
się przewagę płci męskiej oraz rzadszą przynależność
do mniejszości etnicznych.21,28,32
• U młodzieży z fenotypem cukrzycy typu 2 z obecnymi przeciwciałami funkcja komórek ß
jest znacznie gorsza, co skutkuje szybszą progresją
do insulinozależności.28,31,32
Niejasności związane z klasyfikacją choroby
Aby odróżnić cukrzycę typu 1 od cukrzycy typu 2 lekarz musi przeanalizować fakty indywidualnie u każdego pacjenta. Przyczyny trudności w klasyfikacji
obu chorób są następujące:
• w związku z coraz częstszym występowaniem
otyłości w dzieciństwie aż 30% chorych z nowo
rozpoznaną cukrzycą typu 1 (lub cukrzycą
monogenową) może być otyłych, w zależności
od częstości występowania otyłości w danej
populacji
• u znacznej liczby dzieci i młodzieży chorych
na cukrzycę typu 2 w chwili rozpoznania występuje
ketonuria lub kwasica ketonowa2
• w populacji dorosłych cukrzyca typu 2 występuje
często, a dodatni wywiad rodzinny stwierdza się u ≥15% osób w populacjach mniejszości
etnicznych, co ogranicza znaczenie dodatniego
wywiadu rodzinnego
• w momencie rozpoznania cukrzycy oraz w pierwszym roku jej trwania obserwuje się
znaczne podobieństwo wyników oznaczeń
stężenia insuliny lub peptydu C pomiędzy
cukrzycą typu 1 a cukrzycą typu 2. To podobieństwo
wynika z występowania częściowej
remisji (tzw. miesiąc miodowy) w wywołanej
autoimmunizacją cukrzycy typu 1 oraz wpływu
hiperglikemii (glukotoksyczność) i wolnych
kwasów tłuszczowych (lipotoksyczność) upośledzających
wydzielanie insuliny w momencie
wykonywania badań zarówno w cukrzycy
typu 1, jak i cukrzycy typu 2. Ponadto insulinooporność i otyłość zwiększają resztkowe stężenie
peptydu C u otyłych młodocianych chorych
na cukrzycę typu 1. Tego typu badania są więc
raczej bezwartościowe w ostrej fazie choroby.
Jednak utrzymywanie się stężenia peptydu C
powyżej normy dla wieku 12–14 miesięcy po
ustaleniu rozpoznania nie jest typowe dla cukrzycy
typu 1.36
• insulinooporność występuje zarówno w cukrzycy
typu 2, jak i typu 1, jednak patofizjologia
tego zjawiska jest inna, a w cukrzycy typu 2 insulinooporność jest na ogół bardziej nasilona40,41
• oznaczenie autoprzeciwciał związanych z cukrzycą
jest najdokładniejszą metodą identyfikującą
przypadki cukrzycy typu 1. Jednak
badania te mogą mieć ograniczone znaczenie
ze względu na brak standaryzowanych testów,
koszt badania, udział w procesie autoimmunizacyjnym
niezidentyfikowanych do tej pory
przeciwciał oraz zróżnicowaną częstość wykrywania
przeciwciał u chorych na cukrzycę typu 1 pochodzących z różnych grup etnicznych.
Stan przedcukrzycowy: kryteria diagnostyczne (upośledzona tolerancja glukozy i nieprawidłowa glikemia na czczo)
U niektórych osób stężenie glukozy nie spełnia
kryteriów rozpoznania cukrzycy, ale jest zbyt
duże, aby uznać je za prawidłowe. Takie przypadki
ADA określa jako stan przedcukrzycowy, aby
zwrócić uwagę na duże ryzyko rozwoju cukrzycy u tych osób.25
• Upośledzona tolerancja glukozy (IGT) oraz nieprawidłowa
glikemia na czczo (IFG) są stanami
pośrednimi w naturalnym rozwoju zaburzeń
metabolizmu węglowodanów, pomiędzy prawidłową
homeostazą glukozy a cukrzycą.
• IFG oraz IGT nie są pojęciami wymiennymi i reprezentują rożne nieprawidłowości w zakresie
regulacji stężenia glukozy. IFG odnosi
się do zaburzeń metabolizmu węglowodanów w stanie podstawowym, podczas gdy IGT jest
dynamicznym stanem nietolerancji węglowodanów
po obciążeniu standardową porcją glukozy.
42
• U osób spełniających kryteria rozpoznania IGT
lub IFG stężenie glukozy na co dzień może być
prawidłowe, na co wskazują prawidłowe lub bliskie
normy wartości hemoglobiny glikowanej, a u osób z IGT hiperglikemia może występować
wyłącznie podczas OGTT.
• U niektórych osób wartości hemoglobiny glikowanej
mogą być zwiększone, lecz wynik OGTT
jest prawidłowy. Prawdopodobnie odzwierciedla
to przyjmowanie dziennie większej ilości węglowodanów
niż przy standardowym obciążeniu
glukozą.
• U otyłych nastolatków stan przedcukrzycowy
jest często stanem przejściowym, u 60% obserwuje
się przywrócenie prawidłowej tolerancji
glukozy w ciągu 2 lat. Utrzymujący się przyrost
masy ciała jest czynnikiem prognostycznym
przewlekłego stanu przedcukrzycowy i progresji
do cukrzycy.43
• Stan cukrzycowy rozpoznaje się w następujących
sytuacjach:
– IFG: FPG 5,6–6,9 mmol/l (100–125 mg/dl)
– IGT: stężenie glukozy w osoczu po obciążeniu
7,8–11,1 mmol/l (140–199 mg/dl)
– HbA1c 5,8–6,4%.
Oznaczenie należy wykonać w laboratorium
stosującym testy z certyfikatem National Glycohemoglobin
Standardization Program, standaryzowane
zgodnie z DCCT.
Leczenie cukrzycy typu 2 ujawniającej się w wieku młodzieńczym
1) Różnice w leczeniu cukrzycy typu 2 i typu 1
Pojawienie się cukrzycy typu 2 u dzieci i młodzieży
sprawiło, że lekarze mający doświadczenie w postępowaniu z dziećmi i młodocianymi chorymi
na cukrzycę typu 1 muszą zwrócić uwagę
na znaczne różnice w zakresie wyzwań terapeutycznych w tych dwóch chorobach.
• Różnice w statusie społeczno-ekonomicznym:
podczas gdy rozkład cukrzycy typu 1 w populacji jest równomierny niezależnie
od statusu społeczno-ekonomicznego, cukrzyca
typu 2 w krajach rozwiniętych nieproporcjonalnie
częściej występuje u osób mniej zamożnych,
na przykład o niższych dochodach, mających
gorzej wykształconych rodziców czy posiadających
gorsze ubezpieczenie.35 Natomiast w Azji i krajach szybko rozwijających się cukrzycę
typu 2 niewspółmiernie częściej obserwuje się u osób zamożniejszych.
• Starszy wiek: cukrzyca typu 1 występuje w dzieciństwie, kiedy dominujący wpływ
na dziecko mają rodzice, natomiast cukrzyca
typu 2 zwykle występuje w okresie młodzieńczym,
kiedy dominuje wpływ rówieśników.
• Więcej doświadczeń rodzinnych: tylko 5%
rodzin, w których żyje dziecko chore na cukrzycę
typu 1, ma własne doświadczenie związane z występowaniem tej choroby w rodzinie, podczas
gdy takie doświadczenie jest udziałem
ponad 75% rodzin dzieci chorych na cukrzycę
typu 2. U członków tych rodzin częste są niepowodzenia w kontroli masy ciała i glikemii,
co skutkuje występowaniem u nich powikłań i ryzyka poczucia bezsilności.
• Częstość występowania chorób współistniejących i powikłań na wczesnym etapie
cukrzycy: w przeciwieństwie do cukrzycy
typu 1, w której powikłania rozwijają się wiele
lat po rozpoznaniu choroby, większość chorych
na cukrzycę typu 2 będzie cierpieć także na
inne choroby (takie jak stłuszczenie wątroby,
bezdech podczas snu, nadciśnienie tętnicze)35 w momencie rozpoznania cukrzycy. Poza tym
wydaje się, że u chorych na cukrzycę typu 2 powikłania o typie mikro- i makroangiopatii
rozwijają się w szybciej. W związku z tym często
równocześnie z leczeniem nieprawidłowej
glikemii konieczne jest rozpoczęcie leczenia
chorób współistniejących. Aby zmniejszyć częstość
powikłań, należy zwrócić większą uwagę
na choroby współistniejące.21,23,44,45
• Edukacja w zakresie stylu życia: szkolenie w zakresie diety i aktywności fizycznej jest
ważne u wszystkich młodocianych chorych
na cukrzycę, jednak intensywne interwencje
dotyczące zmiany stylu życia stanowią najważniejszy
element leczenia młodzieży chorej
na cukrzycę typu 2.
2) Cele leczenia
• edukacja w zakresie samodzielnego leczenia
cukrzycy
• normalizacja glikemii
• zmniejszenie masy ciała
• zmniejszenie spożycia węglowodanów i liczby
kalorii
• kontrola chorób współistniejących, do których
należą: nadciśnienie tętnicze, dyslipidemia,
nefropatia,
zaburzenia snu i stłuszczenie wątroby
3) Edukacja
(p. także rozdz. Edukacja dzieci i młodocianych chorych na cukrzycę)46
Zarówno wstępna, jak i długoterminowa edukacja w przypadku cukrzycy typu 2 powinna się
koncentrować na zmianach zachowań zdrowotnych
(dieta i aktywność fizyczna), a także, w razie
konieczności, na szkoleniu w zakresie stosowania
doustnych leków hipoglikemizujących i insuliny.
Materiały edukacyjne wykorzystane w badaniu
TODAY dostosowano pod względem wieku i uwarunkowań
kulturalnych do populacji północnoamerykańskiej.
Można się z nimi zapoznać na
ogólnodostępnej stronie internetowej badania
TODAY (portal.bsc.gwu.edu/web/today).
• W optymalnych warunkach leczenie i edukację w zakresie cukrzycy typu 2 powinien prowadzić
zespół składający się m.in. ze specjalisty w dziedzinie żywienia, psychologa i/lub pracownika
socjalnego specjalisty w dziedzinie fizjologii
wysiłku fizycznego.46
• W edukacji chorych na cukrzycę typu 2 większy
nacisk kładzie się na zmiany zachowań dotyczących diety i aktywności fizycznej niż jest
to na ogół wymagane w przypadku cukrzycy
typu 1.
• Edukację powinien prowadzić zespół osób z doświadczeniem i wiedzą z zakresu dietetyki,
ćwiczeń fizycznych i potrzeb psychologicznych
młodzieży chorej na cukrzycę typu 2.
• Edukację należy prowadzić w sposób kulturalny,
delikatny i dostosowany do wieku.
• Większość młodych osób chorych na cukrzycę
typu 2 to nastolatki, dlatego wytyczne ISPAD
dotyczące opieki nad osobami w wieku młodzieńczym
dostosowano do edukacji młodych
osób chorych na cukrzycę typu 2 i ich rodzin.
• Aby chorzy i ich rodziny zrozumieli główne
zasady leczenia cukrzycy typu 2, a także pamiętali o kluczowym znaczenia zmiany stylu
życia w jej skutecznym leczeniu, konieczna jest
edukacja całej rodziny.
• Osoby zajmujące się leczeniem powinny pamiętać,
że obserwowana u niektórych pacjentów
początkowa niepewność co do rozpoznania
cukrzycy typu 1 lub 2 może być przyczyną
dezorientacji i wywoływać niepokój zarówno u chorego, jak i jego rodziny. Aby ten niepokój
zminimalizować, należy podkreślić znaczenie
normalizacji metabolizmu glukozy za pomocą
dowolnej metody leczenia odpowiedniej dla zaistniałych
warunków metabolicznych u danego
chorego niezależnie od „typu” cukrzycy.
4) Zmiana zachowań
Modyfikacja stylu życia jest podstawą leczenia
cukrzycy typu 2. Lekarz powinien zainicjować program
zmiany stylu życia (uwzględniający m.in. dietę i aktywność fizyczną) w momencie rozpoznania
cukrzycy typu 2 u dzieci i młodzieży.47 Konieczne
interwencje to m.in. promowanie zdrowego stylu
życia poprzez zmianę zachowań – dieta, ćwiczenia
fizyczne, normalizacja masy ciała, zaprzestanie
palenia. Interwencje dotyczące stylu życia mogą
mieć korzystny wpływ na zapadalność na cukrzycę u osób z upośledzoną tolerancją glukozy i mogą
skutecznie zmniejszyć zapadalność na cukrzycę
typu 2 u osób z grupy dużego ryzyka.48,49
• Rodzina i dziecko powinni zrozumieć zdrowotne
konsekwencje otyłości i cukrzycy typu 2.
• Aby zaproponować skuteczny plan postępowania,
lekarze muszą wykazać zrozumienie dla
poglądów rodziny na temat zdrowia oraz zachowań
rodziny/społeczności.
• Zmiany należy wprowadzać metodą małych
kroków, równocześnie uświadamiając choremu,
że ich charakter musi być trwały.
• Rodzinę i pacjenta należy przeszkolić w zakresie
monitorowania ilości oraz jakości pożywienia,
zachowań związanych ze spożywaniem
posiłków i regularną aktywnością fizyczną.
• Jak w każdym przypadku zmiany zachowań,
aby osiągnąć sukces, należy stawiać kolejne
wyzwania i stosować system nagradzania.
5) Postępowanie dietetyczne
Konieczne jest zaangażowanie specjalisty w dziedzinie żywienia/dietetyka posiadającego
wiedzę i doświadczenie w leczeniu żywieniowym
młodzieży chorej na cukrzycę. Pożądane jest, aby
taki specjalista miał doświadczenie w zakresie
specyfiki cukrzycy typu 2 u młodych osób. Zalecenia
dietetyczne należy dostosować do warunków
kulturowych i możliwości finansowych rodziny, a następnie przekazać wszystkim osobom
sprawującym opiekę nad chorym. Należy zachęcić
rodzinę do wprowadzenia zmian w diecie zgodnych z zasadami zdrowego żywienia, uwzględniających
indywidualne zalecenia w celu zmniejszenia masy
ciała, zmniejszenia całkowitego spożycia tłuszczów i tłuszczów nasyconych, zwiększenia spożycia
błonnika oraz zwiększenia aktywności fizycznej.
50 Bardziej szczegółowe zalecenia dietetyczne
znajdują się w wytycznych ISPAD dotyczących
postępowania dietetycznego.
Poniżej wymieniono działania, które należy
uwzględnić przy modyfikacji diety.
• W pierwszej kolejności należy się skupić na wyeliminowaniu z diety słodzonych napojów i soków.
Całkowite wyeliminowanie tych napojów i zastąpienie ich wodą, napojami dietetycznymi
lub innymi napojami pozbawionymi kalorii
może spowodować znaczące zmniejszenie masy
ciała.51 Zatwierdzone przez Food and Drug Administration
(FDA) nieodżywcze słodziki mogą
pomóc w ograniczeniu spożycia węglowodanów i energii w ramach strategii kontroli glikemii i masy ciała.51
• Zwiększyć spożycie owoców i warzyw.53
• Ograniczyć spożycie przetworzonej żywności,
dań gotowych i półproduktów.
• Ograniczyć spożycie produktów wytworzonych z rafinowanych cukrów prostych, takich jak syrop
glukozowo-fruktozowy, cukierki.
• Kontrolować wielkość porcji. Jedzenie i przekąski
należy podawać na talerzu lub w misce, a nie spożywać prosto z pudełka lub puszki.
• Ograniczyć spożywanie posiłków poza domem.
• Zmodyfikować dietę azjatycką, która składa się
głównie z posiłków bogatych w węglowodany,
oraz stosowane w niektórych regionach świata
diety o dużej zawartości białka zwierzęcego.
Należy zwiększyć ilość spożywanych świeżych
warzyw, a zmniejszyć ilość bogatego w węglowodany
makaronu, białego ryżu i produktów
zawierających skrobię.
• Zmienić podstawowe produkty żywnościowe –
zrezygnować z wzbogaconego białego ryżu i białej
mąki na rzecz ryżu brązowego i produktów
pełnoziarnistych. Dzięki temu zmniejszy się
indeks glikemiczny posiłków, co sprzyja stopniowemu,
rozłożonemu w czasie narastaniu
glikemii.
• Zmienić rodzinne nawyki dietetyczne:
– ograniczyć dostęp w domu do pokarmów oraz
napojów bogatych w tłuszcz i kalorie
– przeszkolić rodzinę w zakresie interpretacji
informacji podawanych na etykietach
– akcentować wzorce zdrowego odżywiania i aktywności
fizycznej poprzez wyuczenie rodzicielskiego
modelowania zachowań prozdrowotnych i unikanie zbyt restrykcyjnej diety
– zachęcać do pozytywnego wzmacniania wszystkich
osiągniętych celów (np. brak lub minimalny
przyrost masy ciała, zmniejszenie spożycia
wysokokalorycznych napojów) oraz unikać obwiniania
za niepowodzenia
– zalecać spożywanie posiłków zgodnie z planem, w jednym miejscu, bez innych towarzyszących
czynności (oglądania telewizji, uczenia się, czytania,
grania), najlepiej w gronie rodzinnym
– nawiązać współpracę z rodziną, aby móc
uwzględnić zwyczaje żywieniowe wynikające z uwarunkowań kulturowych oraz produkty spożywane w czasie uroczystości rodzinnych i świąt
– zachęcać do prowadzenia dzienników żywienia i aktywności fizycznej, które rozwijają bardziej
świadome odżywianie i podejmowanie aktywności
oraz poprawiają monitorowanie leczenia.
6) Ćwiczenia fizyczne
Ćwiczenia fizyczne są ważną częścią planu
leczenia cukrzycy. Wykazano, że regularne ćwiczenia
poprawiają kontrolę glikemii, zmniejszają
wpływ czynników ryzyka chorób układu krążenia,
pomagają zmniejszyć masę ciała oraz poprawiają
samopoczucie.54-56 Młodzież chorą na cukrzycę
typu 2 należy zachęcać do codziennego umiarkowanego
lub intensywnego wysiłku fizycznego
trwającego co najmniej 60 min (można go podzielić
na kilka krótszych serii). Dla każdego pacjenta i jego rodziny należy przygotować indywidualne,
szczegółowe, uzgodnione i zachęcające zalecenia
dotyczące ćwiczeń fizycznych, uwzględniając
możliwości finansowe rodziny i otoczenia. Należy
wskazać członka rodziny lub przyjaciela, który
mógłby uczestniczyć w aktywności fizycznej razem z pacjentem.
Poniżej wymieniono zagadnienia, które należy
uwzględnić w zaleceniach dotyczących ćwiczeń
fizycznych.
• Wspólne opracowanie możliwego do zrealizowania
codziennego programu ćwiczeń, którego
celem jest ograniczenie czasu spędzanego w pozycji
siedzącej, typowego zjawiska u młodzieży
chorej na cukrzycę typu 2.
• Ograniczenie czasu spędzonego w pozycji
siedzącej (np. oglądania telewizji, spędzania
czasu przy komputerze, na pisaniu smsów lub
na grach wideo).57 Czas spędzony przed telewizorem
lub komputerem powinien być krótszy
niż 2 h dziennie. Korzystanie z urządzeń elektronicznych,
takich jak gry wideo, komputery
czy smartfony, wiąże się ze skróceniem czasu
snu, zwiększeniem masy ciała, stosowaniem
gorszej jakości diety i rzadszym podejmowaniem
aktywności fizycznej.57-59
• Zachęcanie rodziny do ustabilizowania codziennych
aktywności, zwłaszcza do wydłużenia czasu
snu i ograniczenia oglądania telewizji.59-61
• Uwzględnienie problemu czasu spędzonego w pozycji siedzącej podczas odrabiania zadań
domowych oraz znajdowanie sposobów na wypełnienie
przerw w nauce aktywnością fizyczną.
• Promowanie aktywności fizycznej w całej rodzinie.
Codziennie należy podejmować działania
na rzecz zwiększenia aktywności fizycznej, takie
jak korzystanie ze schodów, a nie z windy,
chodzenie pieszo lub jazda rowerem do szkoły i sklepu oraz prace w domu i ogrodzie.
• Zachęcenie do pozytywnego wzmacniania
wszystkich sukcesów i unikanie zawstydzania
dziecka w razie niepowodzeń.
7) Palenie tytoniu
Palenie tytoniu jest szkodliwe dla wszystkich
młodych osób, jednak osoby ze specjalnymi potrzebami
zdrowotnymi są szczególnie wrażliwe
na niekorzystne konsekwencje palenia ze względu
na ich gorszy stan zdrowia, chorobę podstawową
oraz powikłania związane z leczeniem.62
Konieczne jest przeprowadzenie dodatkowych
badań w celu opracowania i oceny skuteczności interwencji
nakierowanych na palenie tytoniu w populacji
młodzieży chorej na cukrzycę, stosowanych w placówkach opieki zdrowotnej. Na każdej wizycie
pacjenta należy zapytać, czy jest osobą palącą i ewentualnie odradzić mu sięganie po tę używkę.
Młodzieży palącej tytoń należy udzielić porady o znaczeniu zaprzestania palenia oraz zapewnić
odpowiednie wsparcie.
8) Monitorowanie glikemii
• Samokontrola glikemii (SMBG)
– W przeciwieństwie do cukrzycy typu 1, istnieją
jedynie ograniczone dane, że SMBG ma wpływ
na kontrolę glikemii u chorych na cukrzycę
typu 2.
– SMBG należy prowadzić regularnie. Częstotliwość
monitorowania należy ustalać indywidualnie
dla każdego pacjenta, na podstawie
stopnia kontroli glikemii i dostępnych środków.
Powinna ona obejmować zarówno oznaczenia
glikemii na czczo, jak i po posiłkach.
– Po osiągnięciu docelowych wartości glikemii
wystarczy wykonywać wybrane oznaczenia
(w warunkach domowych), łącznie z glikemią
na czczo i poposiłkową kilka razy w tygodniu.
Jeżeli wartości stale się zwiększają powyżej
wartości docelowych, należy zalecić częstsze
wykonywanie oznaczeń, ponieważ konieczna
może być modyfikacja leczenia.
– Podczas choroby o ostrym przebiegu oraz po
wystąpieniu objawów hiper- lub hipoglikemii
chorzy powinni częściej wykonywać oznaczenia
glikemii oraz pozostawać w kontakcie z zespołem
leczącym w celu ewentualnego uzyskania
porady.
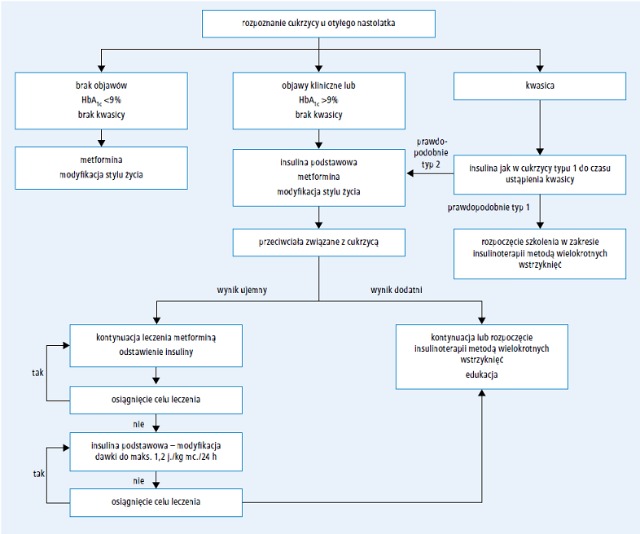
Ryc. Postępowanie w cukrzycy typu 2 u młodzieży - leczenie wstępne i w późniejszym etapie choroby.
• Chorzy leczeni insuliną lub pochodnymi sulfonylomocznika wymagają monitorowania pod kątem bezobjawowej hipoglikemii.
• HbA1c należy oznaczać co najmniej dwa razy w roku, a w przypadku leczenia insuliną lub niedostatecznej kontroli metabolicznej – raz na kwartał.
9) Leczenie farmakologiczne (p. ryc.)
Celem leczenia farmakologicznego cukrzycy typu 2 objawiającej się w wieku młodzieńczym jest zmniejszenie insulinooporności, zwiększenie wydzielania endogennej insuliny lub dostarczenie insuliny egzogennej. Dostępnych jest wiele doustnych leków hipoglikemizujących zarejestrowanych do stosowania u dorosłych, jednak w większości krajów do leczenia nastolatków dopuszczona jest jedynie metformina i insulina. W niektórych krajach do leczenia osób w wieku młodzieńczym zarejestrowane są pochodne sulfonylomocznika. Inne leki doustne opisano poniżej dla informacji, uznając, że w wybranych przypadkach ich zastosowanie u nastolatków może być korzystne. Jednak są one na ogół droższe niż standardowo używane leki, a dane dotyczące ich stosowania w wieku młodzieńczym są ograniczone lub w chwili obecnej w ogóle niedostępne. Aktualnie prowadzi się kilka badań nad nowszymi doustnymi lekami hipoglikemizującymi w leczeniu cukrzycy typu 2 w wieku młodzieńczym, lecz proces rekrutacji do tych badań przebiega powoli i w ciągu wielu następnych lat nie należy oczekiwać żadnych wyników.
• Leczenie wstępne
W leczeniu wstępnym cukrzycy typu 2 objawiającej się w wieku młodzieńczym należy zastosować metforminę i/lub insulinę w monoterapii lub terapii skojarzonej. Specyfika schematu wstępnego leczenia zależy od objawów, stopnia ciężkości hiperglikemii oraz obecności lub braku ketozy/kwasicy ketonowej. Podobnie jak w cukrzycy typu 1, w przypadku obecności objawów klinicznych, zwłaszcza wymiotów, możliwe jest gwałtowne pogorszenie stanu chorego, dlatego konieczne jest szybkie rozpoznanie i wdrożenie leczenia.
– U chorych stabilnych metabolicznie (HbA1c <9, brak objawów) lekiem z wyboru jest metformina w monoterapii. Leczenie należy rozpocząć od dawki 500 mg/24 h przez 7 dni. Dawkę należy zwiększać raz w tygodniu o 500 mg w ciągu 3–4 tygodni aż do uzyskania dawki maksymalnej 1000 mg 2 razy/24 h (lub 2000 mg raz /24 h, jeśli dostępny jest preparat o przedłużonym uwalnianiu).
– Jeżeli chory nie jest wyrównany metabolicznie, konieczne jest zastosowanie insuliny, przynajmniej na wstępnym etapie leczenia. Skuteczne są różne schematy insulinoterapii, lecz kontrolę metaboliczną pozwala często przywrócić podawanie raz/24 h insuliny NPH lub podstawowej (dawka początkowa 0,25–0,5 j./kg mc.) – taka terapia wiąże się z małymi obciążeniami dla pacjenta i jest dobrze tolerowana. Na ogół równocześnie można wprowadzić metforminę, jeżeli u chorego nie stwierdza się kwasicy.
– Przejścia z leczenia insuliną na metforminę w monoterapii można zwykle dokonać po 2–6 tygodniach, zmniejszając dawkę insuliny o 30–50% za każdym razem, gdy zwiększa się dawkę metforminy, tak aby docelowo całkowicie wyeliminować insulinę. Wyniki badania TODAY wskazują, że u 90% młodzieży chorej na cukrzycę typu 2 metformina w monoterapii jest skuteczna w leczeniu wstępnym.34
– Jeżeli w trakcie zmian dawek insuliny i metforminy glikemia pozostaje w zakresach wartości diagnostycznych dla cukrzycy, należy ponownie rozważyć rozpoznanie cukrzycy typu 2 i zintensyfikować zmiany stylu życia.
Celem wstępnego leczenia powinno być uzyskanie wartości HbA1c <6,5%. Jest to prawie zawsze możliwe dzięki metforminie i insulinie podstawowej stosowanych w monoterapii lub w leczeniu skojarzonym. Jeżeli samokontrola glikemii wykazuje, że stężenia glukozy pozostają w zakresach wartości diagnostycznych dla cukrzycy lub poziom HbA1c nie zmniejsza się poniżej 6,5%, należy zweryfikować rozpoznanie cukrzycy typu 2 i ocenić wskazania do intensyfikacji leczenia.
Leczenie w późniejszym etapie choroby
Uzyskanie długotrwałej kontroli glikemii jest
bardziej prawdopodobne raczej przy intensyfikacji
leczenia mającej na celu uzyskanie docelowego odsetka
HbA1c (treat-to-target) niż przy oczekiwaniu
na zwiększenie odsetka HbA1c przed podjęciem
decyzji o intensywniejszym leczeniu (treat-to-failure).
63
• Jeśli w ciągu 3–4 miesięcy leczenia wyłącznie
metforminą nie uda się uzyskać docelowego
odsetka HbA1c <6,5%, należy silnie rozważyć
dodanie insuliny podstawowej.
• Jeśli nie uda się uzyskać takiego poziomu
HbA1c w trakcie leczenia skojarzonego metforminą i insuliną podstawową (w dawce do 1,2 j./
kg mc.), należy dołączyć bolus posiłkowy insuliny, a następnie modyfikować jego dawkę
do czasu uzyskania wartości <6,5%.
• U młodzieży korzystne może być zastosowanie
innych leków doustnych lub we wstrzyknięciach
– dodatkowo lub zamiast insuliny i metforminy, jednak takie metody oceniono w bardzo niewielu badaniach, a większość takich
leków nie jest zarejestrowana w tej grupie
wiekowej.
Metformina
Metformina działa na komórki wątroby, mięśni i tkanki tłuszczowej poprzez kinazę związaną z adenozyno-monofosforanem (AMP), przy czym
głównym narządem docelowym jest wątroba.
• Zmniejsza produkcję glukozy w wątrobie poprzez
hamowanie glukoneogenezy.
• Pobudza wychwyt glukozy zależny od insuliny w mięśniach i tkance tłuszczowej.
• Występujące na początku leczenia zahamowanie
łaknienia może prowadzić do niewielkiego
zmniejszenia masy ciała.
• Przy monoterapii metforminą nie występuje
ryzyko hipoglikemii lub jest ono małe.
• Długotrwałe stosowanie jest związane z redukcją
HbA1c o 1–2%.
• U osób leczonych metforminą mogą występować
działania niepożądane ze strony przewodu pokarmowego
(przemijający ból brzucha, biegunka,
nudności). U większości chorych można je
wyeliminować, powoli zwiększając dawkę leku w ciągu 3–4 tygodni oraz pouczając chorego,
aby zawsze przyjmował lek podczas posiłku.
Działania niepożądane można złagodzić, stosując
preparaty o przedłużonym uwalnianiu.
• Ryzyko wystąpienia kwasicy mleczanowej podczas
leczenia metforminą jest niezwykle małe.
Metforminy nie należy stosować u chorych z upośledzeniem funkcji nerek, niewydolnością
krążenia lub oddechową ani u otrzymujących
radiologiczne środki kontrastowe. W razie wystąpienia
nieżytu żołądkowo-jelitowego należy
czasowo wstrzymać stosowanie metforminy.
• Metformina może znormalizować nieprawidłowości
owulacji u dziewcząt z zespołem wielotorbielowatych
jajników (hiperandrogenizm pochodzenia
jajnikowego) oraz zwiększyć prawdopodobieństwo
zajścia w ciążę.
• Zgodnie z aktualną rejestracją metforminę
można stosować w czasie ciąży.
Insulina
Mimo hiperinsulinemii i insulinooporności suplementacja
insuliny jest na ogół skuteczna w zmniejszaniu
hiperglikemii i uzyskaniu docelowych
wartości glikemii. W przypadku niedostatecznej
kontroli glikemii w trakcie stosowania leków
doustnych, skuteczne leczenie bez konieczności
podawania insuliny do posiłków mogą zapewnić
długo działające bezszczytowe analogi insuliny
lub insulina NPH podana jednorazowo w ciągu
doby.64 Należy kontynuować leczenie metforminą,
aby poprawić wrażliwość na insulinę, a leczenie
nie skojarzone metforminą i insuliną podawaną
raz/24 h u większości nastolatków skutecznie
utrzymuje przez długi czas docelowe wartości glikemii.
Jednak jeśli odsetek HbA1c pozostaje powyżej
wartości docelowej i utrzymuje się poposiłkowa
hiperglikemia, można dodać insulinę szybko lub
krótko działającą.
Główne działania niepożądane insuliny to:
– hipoglikemia – występuje bardzo rzadko u młodzieży
chorej na cukrzycę typu 2, mimo że dawki
insuliny niekiedy są znacznie zwiększone65
– przyrost masy ciała – może być znaczny w tej
populacji po rozpoczęciu leczenia insuliną, jeśli
nie przestrzega się zaleceń dietetycznych,
dlatego należy zwracać szczególną uwagę na
stosowanie odpowiedniej diety i podejmowanie
aktywności fizycznej.
Inne dostępne leki
Pochodne sulfonylomocznika i meglytinid/repaglinid
(w niektórych krajach mogą nie być zarejestrowane u osób <18. rż.):
• Wiążą się z receptorem kompleksu kanału potasowego
zależnego od ATP, powodując jego
zamknięcie, co prowadzi do wydzielania insuliny.
Meglytinid i repaglinid wiążą się z innym
miejscem tego kompleksu.
– Pochodne sulfonylomocznika uwalniają się z miejsc wiązania powoli i wiązanie to utrzymuje
się przez dłuższy czas, dlatego tradycyjne
pochodne sulfonylomocznika wykazują przedłużone
działanie.
– Meglytinid i repaglinid mają pośredni czas dysocjacji i wiązania, dlatego stosuje się je w celu
szybkiego zwiększenia wydzielania insuliny
przed posiłkami.
• U dorosłych stosowanie pochodnych sulfonylomocznika
jest związane ze zmniejszeniem
HbA1c o 1,5–2%.
• Najważniejsze działania niepożądane pochodnych
sulfonylomocznika to:
– hipoglikiemia – w zależności od preparatu może
być ciężka i długo się utrzymywać; wydaje się,
że u młodzieży chorej na cukrzycę typu 2 częściej
obserwuje się hipoglikemię
– zwiększenie masy ciała.
• U dzieci przeprowadzono 1 badanie kliniczne
oceniające pochodne sulfonylomocznika (glimepiryd). Nie wykazano w nim większych korzyści
glimepirydu, w porównaniu z metforminą, przy
czym w grupie leczonej glimepirydem stwierdzono
większy przyrost masy ciała i częstsze
epizody hipoglikemii.66
• Pochodne sulfonylomocznika mogą przyspieszać
utratę funkcji komórek ß, co ostatecznie skutkuje
brakiem kontroli choroby przy stosowaniu
wyłącznie leków doustnych.63
Pochodne tiazolidynodionu (niezarejestrowane u osób <18. rż.)
Pochodne tiazolidynodionu (TZD) zwiększają
wrażliwość na insulinę w mięśniach, tkance
tłuszczowej i wątrobie, wykazując większy wpływ
na wychwyt glukozy przez mięśnie niż pochodne
biguanidu (metformina – przyp. red.). Pochodne
TZD wiążą się z jądrowymi receptorami aktywowanymi
przez proliferatory peroksysomów
(PPAR-γ), które są szeroko rozpowszechnionymi
steroidowymi receptorami sierocymi, szczególnie
licznie występującymi w komórkach tłuszczowych.
Ta aktywacja zwiększa syntezę białek biorących
udział w działaniu insuliny na poziomie jądra komórkowego,
do którego zalicza się wzrost komórki,
różnicowanie tkanki tłuszczowej, regulację aktywności
receptora insulinowego oraz dokomórkowy
transport glukozy. Wiązanie się pochodnych TZD z licznymi receptorami PPAR-γ upośledza wzrost i migrację miocytów w odpowiedzi na czynniki
wzrostowe, co dotyczy także mięśni gładkich ścian
naczyń.
• Długotrwałe leczenie dorosłych jest związane z redukcją HbA1c o 0,5–1,3%.
• Przeprowadzono badanie z randomizacją oceniające
stosowanie rozyglitazonu, jednak nigdy
nie opublikowano jego wyników.
• W badaniu TODAY dodanie rozyglitazonu do leczenia
metforminą zmniejszyło ryzyko rozwoju
insulinozależności o 23%.22
• Pochodne TZD mają różny wpływ na profil lipidowy.
Efekt działania pioglitazonu na LDL jest
korzystniejszy niż rozyglitazonu.
• Działania niepożądane pochodnych TZD
to m.in. zwiększenie masy ciała, niedokrwistość,
zatrzymanie płynów (w tym zastoinowa
niewydolność serca).67,68 Nie stwierdzono, aby
nowsze preparaty wykazywały działanie hepatoksyczne, które obserwowano w trakcie stosowania leków starszej generacji z tej grupy.
• W Stanach Zjednoczonych i Europie urzędy rejestracji
produktów leczniczych nałożyły duże
ograniczenia na stosowanie rozyglitazonu
ze względu na doniesienia o zwiększonym ryzyku
zastoinowej niewydolności serca i zawału
serca.68,69
• Ograniczenia te obecnie już nie obowiązują,
jednak przyszłość pochodnych TZD w leczeniu
cukrzycy typu 2 u dorosłych i młodzieży jest
niejasna.
Inhibitory α-glukozydaz (niezarejestrowane u osób <18. rż.)
Inhibitory α-glukozydaz (akarboza, miglitol [miglitol
jest niezarejestrowany i niedostępny w Polsce
– przyp. red.]) zmniejszają wchłanianie węglowodanów w bliższym odcinku jelita cienkiego
poprzez hamowanie trawienia oligosacharydów,
przez co opóźniają wchłanianie w dalszej części
jelita cienkiego. Zmniejsza to narastanie glikemii
poposiłkowej.
• Długotrwałe stosowanie jest związane z redukcją
HbA1c o 0,5–1%.70
• Ze względu na mechanizm działania leki te
są szczególnie często i skutecznie stosowane w krajach szybko rozwijających się, gdzie węglowodany
stanowią znaczącą część diety.
• U młodzieży nie przeprowadzono żadnych
badań oceniających leczenie inhibitorami
α-glukozydaz.
• Częstym działaniem niepożądanym są wzdęcia,
co sprawia, że większość chorych w wieku młodzieńczym
nie akceptuje tych leków.
Leki pobudzające układ inkretynowy – agoniści receptora peptydu glukagonopodobnego 1 (niezarejestrowane u osób <18. rż.)
Agoniści receptora peptydu glukagonopodobnego
(GLP-1) są szybko wydzielane do krążenia przez
komórki L jelita cienkiego w odpowiedzi na posiłek,
co powoduje zwiększenie wydzielania insuliny
proporcjonalnie do stężenia glukozy we krwi, zahamowanie
wydzielania glukagonu, przedłużenie
opróżniania żołądkowego oraz wywołanie uczucia
sytości. Są one szybko rozkładane przez peptydazę
dipeptydylową
IV (DPP-IV). Okres półtrwania zarówno
wewnątrzpochodnego GLP-1, jak i wstrzykniętych
mimetyków wynosi 2 minuty. W ostatnich
latach w wyniku modyfikacji agonistów GLP-1
uzyskano preparaty o dłuższym czasie działania.
• Leki pobudzające układ inkretynowy podaje się
we wstrzyknięciach podskórnych 2 razy/24 h,
raz/24 h lub raz w tygodniu.
• W badaniach klinicznych przeprowadzonych u dorosłych wykazano zmniejszenie glikemii
na czczo i po posiłkach, zmniejszenie masy ciała
oraz redukcję odsetka HbA1c (0,5–0,8%).
• Do działań niepożądanych zalicza się nudności,
wymioty, biegunkę oraz rzadko występujące
zawroty głowy, ból głowy i objawy dyspeptyczne.
Nasilenie działań niepożądanych na ogół
zmniejsza się wraz z upływem czasu.
• Nie opublikowano żadnych badań oceniających
stosowanie tych leków u młodzieży, lecz aktualnie
kilka badań jest w toku.
Inhibitory DPP-IV (niezarejestrowane u osób <18. rż.)
Inhibitory DPP-IV hamują enzym rozkładający
GLP-1, co powoduje zwiększenie stężenia GLP-1 i wywołuje efekt podobny do analogu GLP-1.
• Inhibitory DPP-IV podaje się doustnie raz
na dobę.
• Długotrwałe stosowanie u dorosłych jest związane z redukcją HbA1c o 0,5%.
• W przeciwieństwie do analogów GLP-1 nie
wpływają na opróżnianie żołądka, uczucie sytości
ani zmniejszenie masy ciała.
• Nie opublikowano żadnych badań oceniających
stosowanie inhibitorów DPP-IV u młodzieży,
lecz kilka badań jest obecnie w toku.
Inhibitory kotransportera 2 glukozy zależnego od jonów sodowych (niezarejestrowane u osób <18. rż.)
Inhibitory kotransporteta 2 glukozy zależnego
od jonów sodowych (SGLT-2) hamują zwrotne
wchłanianie glukozy w kanalikach nerkowych,
co powoduje zwiększone wydalanie glukozy z moczem,
zmniejszenie stężenia glukozy we krwi oraz
zmniejszenie masy ciała. Pierwszy z takich leków
zarejestrowano do leczenia cukrzycy typu 2 u dorosłych.
• Krótkotrwałe stosowanie inhibitorów SLGT-2
wiąże się ze zmniejszeniem odsetka HbA1c w stopniu podobnym do efektu wywoływanego
przez metforminę. Brakuje badań oceniających
długotrwały wpływ na redukcję poziomu HbA1c.
• W badaniach z krótkim okresem obserwacji
zmniejszenie mały ciała sięgało kilku kilogramów.
• Wśród działań niepożądanych wymienia się
nieznacznie częstsze występowanie zakażenia
układu moczowego, szczególnie u nieobrzezanych
mężczyzn.
• Nie przeprowadzono żadnych badań oceniających
stosowanie inhibitorów SGLT u młodzieży.
10) Chirurgia bariatryczna
Chirurgię bariatryczną można rozważyć u młodzieży z chorobami związanymi z otyłością, w tym u chorych na cukrzycę typu 2,71 zwłaszcza gdy
leczenie zachowawcze okazało się nieskuteczne.
Niedawno opublikowane wyniki uzyskane przez
duży zespół amerykańskich ośrodków dziecięcej
chirurgii bariatrycznej wskazują na remisję cukrzycy
typu 2 i innych chorób współistniejących u niemal wszystkich nastolatków, z lepszymi wynikami w zakresie wartości docelowych HbA1c niż
przy leczeniu zachowawczym.72 Jednak ominięcie
żołądka sposobem Roux-en-Y (tradycyjna metoda
chirurgicznego zmniejszania masy ciała) może
się wiązać z poważnymi powikłaniami i zgonem.
Do nowszych technik, które wydają się bezpieczniejsze,
zalicza się założenie opaski na żołądek
(gastric banding) oraz rękawową resekcję żołądka.
Chociaż umieralność i częstość powikłań związanych z leczeniem chirurgicznym u dorosłych
zmniejszyły się w ciągu ostatnich 5 lat, to u dzieci
takie leczenie stosuje się rzadko i można je rozważyć
tylko w ośrodkach, w których pracują osoby doświadczone i nadzorujące wyniki takiego leczenia.
Cukrzyca typu 2 i insulinooporność: choroby współistniejące i powikłania
Insulinooporność to zjawisko patologiczne, definiowane jako zmniejszona odpowiedź na fizjologiczne działanie insuliny i jej konsekwencje w zakresie metabolizmu glukozy, tłuszczów i białek oraz funkcji śródbłonka naczyń krwionośnych. Insulinooporność może wystąpić w wielu tkankach, w tym w wątrobie, mięśniach, tkance tłuszczowej i niektórych obszarach mózgu. Jednak nie wszystkie tkanki są oporne na insulinę, ponieważ niektóre z nich nadal reagują na hiperinsulinemię (np. jajniki i układ współczulny unerwiający mięśnie). W obrębie tkanek może również występować insulinooporność równocześnie z zachowaną wrażliwością na insulinę. Przykładem jest wątroba – oporność na efekty metaboliczne insuliny skutkujące zwiększonym wytwarzaniem glukozy w wątrobie przy równocześnie zachowanej odpowiedzi na insulinę pod postacią zahamowania produkcji białka wiążącego hormony płciowe – skutkiem tego jest zwiększone stężenie wolnych steroidów płciowych, stymulacja insulinopodobnego czynnika wzrostu (IGF-1) i końcowy efekt mitogenny.73
Oporność na insulinę jest zwiększona w trakcie
pokwitania (po jego początkowym okresie), w czasie
ciąży, starzenia się, fazy lutealnej cyklu miesiączkowego, u osób rasy innej niż biała oraz u osób
ze zwiększoną zawartością tkanki tłuszczowej
(całkowitej lub trzewnej), stosujących dietę wysokotłuszczową i prowadzących siedzący tryb życia.
Zwiększone ryzyko wystąpienia insulinooporności
może być związane z niektórymi zdarzeniami
występującymi w trakcie rozwoju. Przedwczesna
adrenarche u dziewcząt (pojawienie się owłosienia
łonowego przed ukończeniem 8. roku życia)
może być pierwszym objawem hiperandrogenizmu w przebiegu PCOS, zaburzenia związanego z insulinoopornością.
74,75 Dzieci z masą urodzeniową
zbyt małą w stosunku do wieku płodowego (SGA)
należą do grupy zwiększonego ryzyka insulinooporności
związanej z ograniczeniem wzrastania
wewnątrzmacicznego, rozwoju trzustki i małą
masą mięśniową. U takich dzieci obserwuje się
również zwiększone ryzyko przedwczesnej adrenarche. U dzieci urodzonych z ciąż powikłanych
otyłością, cukrzycą typu 2 lub cukrzycą ciężarnych
istnieje większe ryzyko masy urodzeniowej
zbyt dużej do wieku płodowego (LGA) oraz insulinooporności.
76 Otyłość i nieaktywny tryb życia w dzieciństwie również zwiększają ryzyko rozwoju
oporności na insulinę.
Zespół insulinooporności obejmuje szereg zaburzeń,
które częściej dotyczą osób z opornością
na insulinę. Wśród tych zaburzeń wymienia się:
• nieprawidłową glikemię (nieprawidłową glikemię
na czczo, upośledzoną tolerancję glukozy,
cukrzycę typu 2)
• nieprawidłowe stężenie lipidów (zwiększone
stężenie triglicerydów, zmniejszone stężenie
cholesterolu HDL-C, małe gęste cząstki LDL)
• zaburzenia funkcji śródbłonka (zwiększone
przyleganie komórek jednojądrowych, zwiększone
stężenie białek adhezyjnych rozpuszczonych w osoczu i asymetrycznej dimetyloargininy,
upośledzenie rozszerzania naczyń zależnego
od śródbłonka)
• większe stężenie czynników sprzyjających
krzepnięciu krwi (inhibitor aktywatora plazminogenu 1 i fibrynogen)
• zmiany hemodynamiczne (większa aktywność
układu współczulnego, zatrzymywanie sodu
przez nerki)
• stan zapalny (zwiększone stężenie białka C-reaktywnego,
liczby leukocytów itd.)
• zwiększone stężenie kwasu moczowego w osoczu
• zwiększone gromadzenie tłuszczu w komórkach
wątroby i komórkach mięśniowych
• zaburzenia funkcji mitochondriów
• hiperandrogenizm pochodzenia jajnikowego
• zaburzenia oddychania podczas snu.
W wyniku tych zaburzeń związanych z insulinoopornością
osoby, u których stwierdza się oporność
na insulinę, są narażone na większe ryzyko
wystąpienia klinicznie jawnej cukrzycy typu 2,
chorób układu krążenia, nadciśnienia tętniczego,
PCOS, NAFLD, nefropatii, obturacyjnego bezdechu
podczas snu i niektórych nowotworów. Taki
pogląd, że oporność na insulinę wiąże się z grupą
zaburzeń, różni się od koncepcji zespołu metabolicznego,
definiowanego pięcioma swoistymi kryteriami
związanymi z insulinoopornością (otyłość,
podwyższone ciśnienie tętnicze krwi, nieprawidłowa
glikemia na czczo, duże stężenie triglicerydów,
małe stężenie cholesterolu HDL) wybranymi pierwotnie
przez autorów raportu Adult Treatment Panel
III na podstawie zwiększonego ryzyka chorób
układu krążenia u dorosłych.77
W przeciwieństwie do definicji zespołu metabolicznego u dorosłych, nadal brakuje standardowej
definicji tego zespołu u dzieci – do tej pory u dzieci stosowano ponad 46 różnych definicji.78 W 2007 roku International Diabetes Federation
opublikowała własną definicję zespołu metabolicznego u dzieci i młodzieży.79 Zalecono zastosowanie
następujących kryteriów:
1) U dzieci w wieku od 6 do <10 lat: otyłość (definiowana
jako obwód talii ≥90. centyla), następnie
należy dokonywać dalszych pomiarów w zależności od wywiadu rodzinnego.
2) U dzieci w wieku od 10 do <16 lat: otyłość (definiowana
jako obwód talii ≥90. centyla), wraz z kryteriami dla dorosłych dotyczących stężenia
triglicerydów, cholesterolu HDL, ciśnienia
tętniczego i glikemii. U osób w wieku ≥16 lat
zaleca się stosowanie obecnych kryteriów International
Diabetes Federation dla dorosłych.
Jeżeli zastosuje się taką definicję, częstość występowania
zespołu metabolicznego gwałtownie
się zwiększa wraz z coraz częstszym występowaniem
otyłości u dzieci i ogólnoświatową tendencją
do prowadzenia siedzącego trybu życia. Jeżeli
chodzi o epidemiologię otyłości w krajach zachodnich, u dzieci zapadalność zwiększyła się ponad
2-krotnie na przestrzeni życia ostatniego pokolenia.
Wyniki badań wskazują, że w populacji młodzieży z otyłością odsetek osób z zespołem metabolicznym
mieści się w zakresie 19–35%, natomiast w grupach z prawidłową masą ciała wynosi <2%.
Szanse rozwinięcia się zespołu metabolicznego u otyłych chłopców i dziewcząt były odpowiednio
46–67 i 19–22 razy większe niż u młodzieży z prawidłową
masą ciała.80
Choroby współistniejące, typowe dla zespołu
insulinooporności, często można stwierdzić już w momencie rozpoznania cukrzycy typu 2 lub w jej wczesnym okresie. Badania w kierunku
ich występowania należy wykonywać wcześniej
niż w cukrzycy typu 1, gdzie zaburzenia te mają
na ogół charakter powikłań długotrwałej cukrzycy, a nie chorób współistniejących.81-83 Diagnostykę
powikłań/chorób współistniejących bardziej szczegółowo
opisano w rozdziale dotyczącym mikroi
makroangiopatycznych
powikłań cukrzycy.84
Otyłość
Otyłość ma niekorzystny wpływ na chorobowość niezależnie od efektów związanych z insulinoopornością i cukrzycą.85-94 Poza tym zmniejszenie masy ciała i ćwiczenia fizyczne zmniejszają insulinooporność i poprawiają kontrolę glikemii. Przesunięcie do wyższej lub niższej kategorii BMI w okresie dzieciństwa wpływa na wartości innych czynników ryzyka chorób układu, odpowiednio zwiększając lub zmniejszając ryzyko wystąpienia takich chorób,95 a u amerykańskich nastolatków chorych na cukrzycę typu 2 średni znormalizowany wskaźnik masy ciała (BMI z-score) wynosi 2,15.35 Dlatego ocenę BMI i wzorca zwiększania masy ciała należy uznać za rutynową procedurę w monitorowaniu cukrzycy typu 2 u młodzieży.
Nadciśnienie tętnicze
Nadciśnienie tętnicze wiąże się z zaburzeniami
funkcji śródbłonka, małą podatnością tętnic oraz
zwiększonym ryzykiem chorób układu krążenia i nerek.96 Co więcej, badanie UK Prospective
Diabetes Study (UKPDS) wykazało, że ścisła
kontrola ciśnienia tętniczego u dorosłych chorych
na cukrzycę typu 2 zmniejszyła ryzyko powikłań
mikro- i makroangiopatycznych co najmniej w takim samym stopniu jak kontrola glikemii.97 W badaniu TODAY stwierdzono, że nadciśnienie
tętnicze występowało u 13,6% osób z grupy 699
amerykańskich nastolatków chorych na cukrzycę
(mediana czasu trwania choroby wynosiła 7 miesięcy).
35 W ciągu średnio 3,9 roku obserwacji odsetek
ten zwiększył się do 33,8%.23 Wśród uczestników
badania TODAY płeć męska i większy BMI
wiązały się z istotnie większym ryzykiem nadciśnienia
tętniczego. Eppens i wsp.98 zaobserwowali,
że w Australii nadciśnienie tętnicze występuje
jeszcze częściej – w ciągu 1,3 roku od rozpoznania
cukrzycy typu 2 nadciśnienie tętnicze stwierdza
się u 36% młodzieży. Poza tym według badania
SEARCH for Diabetes in Youth Study (SEARCH)
obejmującego amerykańską młodzież dłużej chorującą
na cukrzycę, nadciśnienie tętnicze stwierdzono u 65% nastolatków chorych na cukrzycę
typu 2.99,100 Nadciśnienie tętnicze w przebiegu
cukrzycy typu 2 wiąże się z zatrzymaniem sodu
przez nerki, czego konsekwencją jest zatrzymanie
płynów, upośledzenie rozszerzania naczyń
krwionośnych stymulowanego przez tlenek azotu, a zatem większy opór naczyń, oraz zwiększona
stymulacja układu współczulnego przez hiperinsulinemię.
Ponadto u chorych na cukrzycę typu 2 może istnieć genetyczna predyspozycja do rozwoju
nadciśnienia tętniczego, która jest związana z genotypem
konwertazy angiotensyny i zwiększoną
aktywnością układu renina–angiotensyna.101
• Ciśnienie tętnicze należy mierzyć na każdej
wizycie – należy dobrać odpowiedni mankiet, a w interpretacji wyniku należy uwzględnić
płeć, wzrost i wiek.
• Jeżeli wartości ciśnienia tętniczego zmierzonego
3-krotnie utrzymują się na poziomie 95. centyla
lub go przekraczają, należy zastosować
leczenie wstępne polegające na zmniejszeniu
masy ciała, ograniczeniu soli w diecie i zwiększeniu
aktywności fizycznej.
• Jeżeli po upływie 6 miesięcy ciśnienie tętnicze
nadal przekracza 95. centyl, należy rozważyć
zastosowanie ACE w celu obniżenia ciśnienia
tętniczego do wartości <90. centyla.102
– Należy pamiętać, że stosowanie ACE w I trymestrze
ciąży u kobiet bez cukrzycy powodowało
powstawanie poważnych wad rozwojowych u płodu.
• W przypadku nietolerancji ACE z powodu działań
niepożądanych (głównie kaszel) jako lek
drugiego wyboru często stosuje się antagonistę
receptora aniotensyny.47,102-105
• Jeżeli nie uda się osiągnąć normalizacji ciśnienia
tętniczego w trakcie stosowania jednego
leku, konieczna może być terapia skojarzona
polegająca na dodaniu na przykład antagonisty
kanału wapniowego lub diuretyku.
• U chorych z nadciśnieniem tętniczym należy
wykonać badanie USG nerek i badanie echokardiograficzne.
96
Nefropatia
Albuminurię (mikro- lub makroalbuminurię) w momencie rozpoznania cukrzycy stwierdza się u znacznego odsetka nastolatków chorych na cukrzycę
typu 2, który zwiększa się wraz z czasem
trwania choroby.24 W badaniu TODAY w grupie
699 młodych osób chorych na cukrzycę typu 2 (mediana czasu trwania choroby 7 miesięcy) mikroalbuminurię
stwierdzono u 6,3%, a odsetek
ten zwiększył się do 16,6% do 36. miesiąca obserwacji.
23,35 Większe stężenie HbA1c wiązało się z istotnie większym ryzykiem rozwoju mikroalbuminurii.
Podobne wyniki uzyskano w mniejszych
badaniach obejmujących Indian i młodzież należącą
do mniejszości etnicznych zamieszkujących
Stany Zjednoczone, a także rdzennych mieszkańców
Kanady oraz młodych Maorysów,15,106 a makroalbuminurię wykryto u 16% młodych
Indian po 10 latach obserwacji.107,108 W badaniu
przeprowadzonym w kanadyjskiej prowincji Manitoba u nastolatków z mikroalbuminurią ryzyko
rozwoju niewydolności nerek było 9-krotnie
większe od ryzyka obserwowanego w grupie bez
mikroalbuminurii.109 Zatem obecność mikroalbuminurii
była silnym czynnikiem prognostycznym
wystąpienia w przyszłości niewydolności
nerek. W cukrzycy typu 2 objawiającej się w wieku młodzieńczym częstość występowania
mikro- i makroalbuminurii jest większa, a progresja
nefropatii jest szybsza niż w przypadku
cukrzycy typu 1 we wszystkich badanych populacjach. U 31 (3%) z 1065 Japończyków, u których
cukrzycę typu 2 rozpoznano przed ukończeniem
30. roku życia, średnio w wieku 35 lat rozwinęła
się niewydolność nerek wymagająca dializoterapii.
110 Czynniki wpływające na progresję to czas
trwania cukrzycy, odsetek HbA1c i wartość rozkurczowego
ciśnienia tętniczego. Poza tym zapadalność
na nefropatię w grupie, w której cukrzycę
rozpoznano w wieku 10–19 lat, była 2-krotnie
większa niż u chorych na cukrzycę typu 1 z tej
samej populacji, nawet po uwzględnieniu czasu
trwania choroby.111
• Mikro- i makroalbuminuria mogą być obecne w momencie rozpoznania cukrzycy.
• Albuminurię należy oznaczyć przy ustalaniu
rozpoznania cukrzycy, a następnie powtarzać
co roku.
• ADA stosuje następujące definicje mikroalbuminurii:
– wskaźnik albumina/kreatynina w pojedynczej
próbce moczu 30–299 mg/g (preferowana)
– wydalanie albuminy z moczem 20–199 µg/min
oznaczane w nocnej lub 24-godzinnej zbiórce
moczu.
• Przyczyną zwiększenia wartości mogą być ćwiczenia
fizyczne, palenie tytoniu, miesiączka i pozycja stojąca, dlatego utrwaloną nieprawidłową
mikroalbuminurię można rozpoznać po
uzyskaniu dwóch nieprawidłowych wyników w trzech kolejnych badanych próbkach pobieranych w różnych dniach.
– Serię badań należy przeprowadzić rano, niezwłocznie
po wstaniu z łóżka, ponieważ u młodzieży
często występuje białkomocz ortostatyczny o łagodnym charakterze.
• Należy wykluczyć niezwiązane z cukrzyca
przyczyny chorób nerek oraz przeprowadzić
konieczne konsultacje, szczególnie jeśli obecna
jest makroalbuminuria (wskaźnik albumina/
kreatynina >300 mg/g).
• Lekami z wyboru są ACE ze względu na ich
korzystny efekty w zapobieganiu nefropatii cukrzycowej,
nawet jeśli ciśnienie tętnicze jest
prawidłowe.2
• Albuminurię należy oceniać co 3–6 miesięcy, a dawkowanie leków należy korygować aż
do uzyskania prawidłowej wartości (jeśli to
możliwe) wskaźnika albumina/kreatynina.
Dyslipidemia
Hipertriglicerydemia i zmniejszone stężenie cholesterolu
HDL to typowe cechy dislipidemii charakterystycznej
dla insulinooporności i cukrzycy
typu 2. W badaniu TODAY, w okresie kilku miesięcy
od rozpoznania cukrzycy małe stężenie cholesterolu
HDL stwierdzono u 79,8% nastolatków
chorych na cukrzycę typu 2, a duże stężenie triglicerydów
– u 10,2%.35 Wynik badania SEARCH
wskazują, że w grupie 2096 amerykańskich nastolatków
dłużej chorujących na cukrzycę typu 2, u 73% z nich wykryto małe stężenie HDL, a hipertriglicerydemię u 60–65%.112 Wśród Indian plemienia
Pima Indians hipercholesterolemię w momencie
rozpoznania cukrzycy stwierdzono u 18%
uczestników badania.107 W populacji rdzennych
mieszkańców Kanady w grupie 99 nastolatków
chorych na cukrzycę typu 2 stężenie całkowitego
cholesterolu, cholesterolu LDL, triglicerydów i apolipoproteiny B przekraczało 75. centyl odpowiednio
u: 60, 41, 43 i 43% uczestników, a małe
stężenie cholesterolu HDL stwierdzono u 35%.108 W grupie 68 młodych Australijczyków chorujących
na cukrzycę krócej niż 3 lata zwiększone stężenie
całkowitego cholesterolu stwierdzono u 32%, a hipertriglicerydemię u 53%.98 Natomiast na Tajwanie
hipercholesterolemię obserwowano u 27%
osób w wieku młodzieńczym chorych na cukrzycę
typu 2.11 Inne nieprawidłowości to zwiększone stężenie
lipoprotein o bardzo małej gęstości (VLDL),
zwiększone stężenie cholesterolu LDL, zwiększone
stężenie lipoproteiny (a) oraz zwiększone stężenie
małych gęstych cząstek LDL. Zmniejszenie
aktywności lipazy lipoproteinowej, zwiększenie
dystrybucji lipoprotein i ich oksydacja powodują
przekształcanie lipoprotein do form bardziej aterogennych.
• Badanie w kierunku dyslipidemii należy przeprowadzić
wkrótce po ustaleniu rozpoznania,
gdy osiągnie się prawidłową kontrolę glikemii, a następnie powtarzać co roku.113-115
• Wartości docelowe to:
– stężenie cholesterolu LDL <2,6 mmol (100 mg/dl),
cholesterolu HDL >35 mg/dl (0,91 mmol/l)
– stężenie triglicerydów <150 mg/dl (1,7 mmol/l).
• Jeżeli stężenie cholesterolu LDL przekracza
wartość docelową, należy zoptymalizować
kontrolę glikemii, zalecić dietę zgodnie z wytycznymi
AHA (dieta II etapu [dobowa zawartość
cholesterolu w diecie <200 mg, tłuszcze
nasycone <7% wszystkich kalorii oraz <30%
kalorii uzyskanych z tłuszczów]) oraz zachęcić
do podejmowania wysiłku fizycznego.114
• Profil lipidowy należy oznaczać co 6 miesięcy.
Jeżeli utrzymuje się zwiększone stężenie cholesterolu
LDL, konieczne są dodatkowe działania:
– stężenie cholesterolu LDL 100–129 mg/dl: optymalizacja
postępowania niefarmakologicznego;
– stężenie cholesterolu LDL >130 mg/dl: rozpoczęcie
leczenia farmakologicznego, jako wartość
docelową należy przyjąć stężenie <130 mg/dl,
optymalnie <100 mg/dl.
• Lekiem pierwszego wyboru powinny być statyny,
których stosowanie u dzieci i dorosłych
oceniono jako bezpieczne i skuteczne,84 aczkolwiek
brakuje danych dotyczących bezpieczeństwa
długotrwałego leczenia.
• Leczenie statynami należy rozpocząć od najmniejszej
dostępnej dawki. Zwiększając dawkę,
należy uwzględnić stężenie cholesterolu LDL i ryzyko wystąpienia działań niepożądanych.
• Jeżeli pacjent zgłosi utrzymujący się ból/tkliwość
mięśni, lek należy odstawić, a chorego
objąć obserwacją pod kątem ustępowania objawów.
• Statyn nie wolno stosować w czasie ciąży, dlatego u nastolatek aktywnych seksualnie takie
leczenie należy rozważać bardzo ostrożnie, dokładnie
omawiając związane z nim ryzyko.
• Aktualne wytyczne nie zalecają normalizacji
stężenia triglicerydów za pomocą leków w celu
profilaktyki chorób układu krążenia.
• Jeżeli stężenie triglicerydów przekracza
150 mg/dl, należy się skupić na optymalizacji
kontroli glikemii, ograniczeniu zawartości
tłuszczów i cukrów prostych w diecie oraz osiągnięciu
pożądanej masy ciała.
• Jeżeli stężenie triglicerydów na czczo przekracza
400–600 mg/dl, należy rozważyć zastosowanie
fibratów ze względu na istotnie zwiększone
ryzyko zapalenia trzustki. Celem terapii
powinno być uzyskanie stężenia <150 mg/dl.
• U młodzieży nie należy stosować leków w celu
normalizacji małego stężenia cholesterolu HDL,
pacjentów należy natomiast zachęcać do podejmowania
wysiłku fizycznego i do zdrowej diety.
Miażdżyca i zaburzenie funkcji śródbłonka
Hiperglikemia, dyslipidemia i nadciśnienie tętnicze to czynniki sprzyjające przyspieszeniu procesu miażdżycowego u chorych na cukrzycę typu 2, wraz ze stresem oksydacyjnym, glikacją białek naczyń krwionośnych i zaburzeniami funkcji płytek krwi i zaburzeniami krzepnięcia. Upośledzenie rozszerzania naczyń zależnego od śródbłonka to kolejny czynnik przyspieszający rozwój miażdżycy w przebiegu cukrzycy typu 2. Nieprawidłowa funkcja śródbłonka jest wczesnym sygnałem zwiększonego ryzyka chorób układu krążenia i jest czynnikiem prognostycznym incydentów sercowo-naczyniowych. 81 Takie zaburzenia obserwuje się u otyłych dzieci i zależą one od stopnia otyłości i oporności na insulinę. Poza tym u młodzieży chorej na cukrzycę typu 2 stwierdza się przerost lewej komory serca,116 zaburzenia funkcji serca, mniejszą maksymalną wydolność wysiłkową41 i większą sztywność tętnic117 – wszystkie te zaburzenia są czynnikami prognostycznymi wczesnych powikłań ze strony układu krążenia i umieralności.
Zespół wielotorbielowatych jajników
PCOS coraz częściej rozpoznaje się u nastolatków
jako jedną ze składowych zespołu insulinooporności. U nastolatek z PCOS zużycie glukozy pod wpływem
insuliny jest o około 40% mniejsze niż w grupie
kontrolnej bez hiperandrogenizmu odpowiednio
dobranej pod względem składu ciała.118 Istnieje
niewiele danych na temat dokładnej częstości występowania
PCOS u dziewcząt chorych na cukrzycę
typu 2, lecz w 1 badaniu zespół ten stwierdzono u 8,3% ze 157 dorosłych kobiet w wieku rozrodczym
chorych na cukrzycę typu 2.119 Brak miesiączek
może zwiększyć odległe ryzyko wystąpienia raka
trzonu macicy, a PCOS zwiększa ryzyko chorób
układu krążenia w okresie całego życia.120
• U każdej nastolatki chorej na cukrzycę typu 2 należy zebrać wywiad dotyczący miesiączek –
zarówno w trakcie diagnostyki cukrzycy, jak i na każdej wizycie kontrolnej.
• Należy rozważyć diagnostykę w kierunku
PCOS, jeżeli u pacjentki stwierdza się pierwotny
lub wtórny brak miesiączki, hirsutyzm i trądzik o dużym nasileniu.
• PCOS rozpoznaje się na podstawie obecności
zaburzeń miesiączkowania (brak miesiączki
lub rzadkie miesiączki) wraz z klinicznymi lub
biochemicznymi wskaźnikami hiperandrogenizmu.
Dodatkowo mogą być obecne wielotorbielowate
jajniki.121
• Zmniejszenie insulinooporności poprzez zmniejszenie
masy ciała, wysiłek fizyczny i leczenie
metforminą może poprawić funkcję jajników i zwiększyć płodność.
• Nastolatki chore na cukrzycę leczoną farmakologicznie
należy poinformować, że w przebiegu
leczenia może dojść do zwiększenia płodności,
dlatego konieczne może być stosowanie metod
zapobiegających zajście w ciążę.
Niealkoholowa choroba stłuszczeniowa wątroby
Stłuszczenie wątroby występuje u 25–50% młodzieży
chorej na cukrzycę typu 2, a bardziej zaawansowane
postacie NAFLD, takie jak niealkoholowe
stłuszczenie wątroby (NASH), są coraz
częstsze i wiążą się z progresją do marskości,
nadciśnienia wrotnego i niewydolności wątroby.
122-124 NAFLD jest obecnie najczęstszą przyczyną
przewlekłych zaburzeń funkcji wątroby u otyłych osób w wieku młodzieńczym,125 a w Stanach
Zjednoczonych jest najczęstszą przyczyną
przeszczepiania wątroby u dorosłych. W Stanach
Zjednoczonych NAFLD występuje z największą
częstością u Latynosów, drugą pod względem wielkości
chorobowość stwierdza się w populacji osób
rasy białej niebędących Latynosami, natomiast u Afroamerykanów NAFLD występuje istotnie
rzadziej.124,126 Jednak wskaźniki te oszacowano
na podstawie zwiększonej aktywności enzymów
wątrobowych i są one prawdopodobnie zaniżone w odniesieniu do częstości występowania stłuszczenia
wątroby u młodzieży chorej na cukrzycę
typu 2, ponieważ stłuszczenie występuje częściej
niż zwiększona aktywność enzymów wątrobowych, a aktywność tych enzymów może być prawidłowa
mimo obecnego stłuszczenia.127
NAFLD wiąże się z opornością na insulinę,
czego skutkiem jest oporność na antylipolityczne
działanie insuliny na tkankę tłuszczową i w dalszej
kolejności zwiększenie stężenia wolnych kwasów
tłuszczowych, które zaburza funkcje mitochondriów i wywołuje działanie lipotokyczne. Poza
tym u osób z NAFLD dochodzi do gromadzenia
ektopowej tkanki tłuszczowej w mięśniu sercowym i trzustce.128 U otyłych nastolatków obecność
zespołu metabolicznego jest czynnikiem prognostycznym
IGT i NAFLD,41 a cukrzyca typu 2 jest
niezależnym czynnikiem prognostycznym włóknienia
wątroby.129
Redukcja masy ciała wiąże się ze zmniejszeniem
nasilenia NAFLD. Wykazano, że u nastolatków z insulinoopornością leczenie metforminą
wpływa korzystnie na aktywność enzymów wątroby i nasilenie stłuszczenia wątroby.41 W badaniu
TODAY konieczność trwałego zmniejszenia dawki
leku lub jego odstawienia ze względu na zwiększenie aktywności enzymów wątrobowych najrzadziej
stwierdzano w grupie leczonej metforminą wraz z rozyglitazonem.65 Zatem wygląda na to, że leki,
które zmniejszają insulinooporność w przebiegu
cukrzycy typu 2, zmniejszają również nasilenie
NAFLD, dlatego są one standardową metodą leczenia
nastolatków chorujących zarówno na cukrzycę
typu 2, jak i na NAFLD. Jednak ze względu
na możliwość progresji do NASH, włóknienia i marskości wątroby, u młodzieży chorej na cukrzycę
typu 2 zaleca się stałe monitorowanie aktywności
enzymów wątrobowych i skierowanie
na biopsję, jeśli wartości te utrzymują się znacznie
powyżej wartości prawidłowych mimo zmniejszenia
masy ciała i/lub leczenia farmakologicznego
cukrzycy.
Uogólniony stan zapalny
Zwiększone stężenie białka C-reaktywnego, cytokin zapalnych i zwiększona liczba leukocytów u otyłych nastolatków wiążą się ze zwiększonym ryzykiem chorób układu krążenia w wieku dorosłym. 92,93 Stan zapalny odgrywa kluczową rolę w patogenezie przewlekłej choroby nerek związanej z cukrzycą,130 retinopatii cukrzycowej,131 zaburzeń funkcji komórek ß132,133 i innych chorób związanych z cukrzycą. Cytokiny zapalne (m.in. TNF-α i IL-6) wydzielane przez tkankę tłuszczową u otyłych osób upośledzają odpowiedź narządów docelowych na insulinę. Dodatkowo zidentyfikowano nowe cząsteczki wpływające na lokalną i ogólnoustrojową reakcję zapalną,134 pojawiają się również doniesienia o roli aktywowanych komórek układu odpornościowego.135,136
Obturacyjny bezdech podczas snu
Obturacyjny bezdech podczas snu jest częstym
zaburzeniem u otyłej młodzieży, jednak brakuje
dobrych danych na temat częstości jego występowania u dzieci chorych na cukrzycę typu 2. Prawdopodobnie
jest ona duża, ponieważ obturacyjny
bezdech podczas snu stwierdza się u 70–90% dorosłych
chorych na cukrzycę typu 2.137,138 Obturacyjny
bezdech podczas snu nie tylko pogarsza
jakość snu i zwiększa senność w ciągu dnia, ale
także posiada pewne następstwa kliniczne, takie
jak nadciśnienie tętnicze, przerost lewej komory
serca oraz zwiększone ryzyko chorób nerek i układu
krążenia.
• Grupa robocza The International Diabetes
Federation Taskforce on Epidemiology and
Prevention silnie zaleca, aby pracownicy placówek
opieki zdrowotnej zajmujący się chorymi
na cukrzycę typu 2 brali pod uwagę możliwość
występowania obturacyjnego bezdechu podczas
snu u swoich pacjentów.139
• Badaniem przesiewowym w kierunku występowania
obturacyjnego bezdechu podczas snu u młodzieży chorej na cukrzycę typu 2 może być
wywiad na temat takich objawów, jak chrapanie,
jakość snu, bezdechy, poranny ból głowy,
senność w ciągu dnia, częste oddawanie moczu w nocy i mimowolne oddawanie moczu.
• Jeżeli objawy wskazują na obturacyjny bezdech
podczas snu, rozpoznanie należy potwierdzić
za pomocą odpowiednich badań i skierować
pacjenta do specjalisty zajmującego się zaburzeniami
snu.
Depresja
Młodzież chora na cukrzycę typu 2 jest narażona
na zwiększone ryzyko dużej depresji,140-144 co wiąże
się z niedostatecznym przestrzeganiem zaleceń
dotyczących leczenia cukrzycy. Objawy depresji
to m.in. obniżenie nastroju, znaczne zmniejszenie
zainteresowania, odczuwania przyjemności,
większe lub mniejsze łaknienie, bezsenność lub
nadmierna senność, pobudzenie lub osłabienie
psychoruchowe, zmęczenie, brak energii, poczucie
braku wartości, nawracające myśli o śmierci.
• Młode osoby w momencie rozpoznania cukrzycy
typu 2 należy ocenić pod kątem objawów depresji.
Ocenę tę należy powtarzać okresowo,
szczególnie u pacjentów często zgłaszających
się na oddziały ratunkowe lub z niedostateczną
kontrolą glikemii.
• Chorego z objawami depresji należy skierować
do odpowiedniego specjalisty mającego doświadczenie w leczeniu depresji u młodzieży.140
Inne problemy zdrowotne związane z otyłością i cukrzycą typu 2
• Dolegliwości ze strony narządu ruchu wynikające
ze zmniejszonej aktywności fizycznej145,146
• Zapalenie trzustki
• Zapalenie pęcherzyka żółciowego
• Rzekomy guz mózgu (pseudotumor cerebri)
• Owrzodzenia tkanek miękkich
U dorosłych w 5. dekadzie życia, którzy zachorowali
na cukrzycę w wieku młodzieńczym, istotnie
częściej występują makroangiopatie, u wielu z nich stwierdza się chorobę niedokrwienną serca
(12,6%), udar mózgu (4,3%) oraz jakiekolwiek
powikłanie makroangiopatyczne (14,4%), a 11% z nich umiera.147 Poza tym wszystkie te punkty
końcowe występowały istotnie częściej niż u chorych
na cukrzycę typu 1 w podobnej grupie wiekowej,
mimo że stopień kontroli glikemii i czas trwania
choroby był podobny. Szacuje się, że u młodzieży i młodych dorosłych chorych na cukrzycę
typu 2 średnia oczekiwana długość życia jest krótsza o około 15 lat, a do 5. dekady życia u takich
chorych mogą się rozwinąć przewlekłe, poważne
powikłania.148 W związku z tym koniecznie należy
stosować kompleksowy program leczenia, który
obejmuje wczesną i agresywną kontrolę powikłań
cukrzycy oraz czynników ryzyka chorób układu
krążenia, aby w ten sposób zmniejszyć ryzyko powikłań i wczesnego zgonu w dalszym okresie życia.
Badania przesiewowe w kierunku cukrzycy typu 2 u młodzieży z grupy dużego ryzyka
W przeciwieństwie do wychwytywania przypadków
cukrzycy w wybranej populacji młodzieży, u której istnieje umiarkowane lub duże podejrzenie
cukrzycy ze względu na objawy kliniczne,
badania przesiewowe odnoszą się do szeroko zakrojonych
badań populacji lub poszczególnych osób
spełniających określone kryteria. W pierwszym
przypadku wykonywanie badań jest niezbędne w ocenie indywidualnych pacjentów, natomiast w drugim jest to uzasadnione tylko w wybranych
okolicznościach.149 Ogólne uzasadnienie prowadzenia
badań przesiewowych w odniesieniu do cukrzycy
typu 2 u młodzieży jest następujące:
• Choroba występuje na tylke często, że ponoszenie
kosztów badań przesiewowych jest uzasadnione.
– Nie jest jasne, czy dotyczy to większości populacji. W Stanach Zjednoczonych przeprowadzono
badania przesiewowe w populacji młodzieży z grupy dużego ryzyka należącej do mniejszości
etnicznych – kontrolę glikemii na czczo i po obciążeniu wykonano w wieku szczytowej
wykrywalności cukrzycy typu 2. Cukrzycę
typu 2 stwierdzono u <1% osób.88 Nadal nie
wiadomo, czy taka częstość nierozpoznanej
cukrzycy w wybranych populacjach młodzieży
uzasadnia prowadzenie badań przesiewowych.
– Jeżeli choroba występuje rzadko, większość nieprawidłowych
wyników testów będą stanowić wyniki
fałszywie dodatnie. Będzie to stwarzać konieczność
przeprowadzenia dodatkowych badań,
co należy uwzględniać przy kalkulacji kosztów.
• Choroba ma poważne konsekwencje w odniesieniu
do powikłań i umieralności.
– Stwierdzenie to niewątpliwie odnosi się do cukrzycy
typu 2 u młodzieży, ponieważ jest ona
związana z występowaniem czynników ryzyka
chorób układu krążenia i niewydolności nerek.
• Choroba cechuje się długim okresem bezobjawowym,
podczas którego można już wykryć
nieprawidłowości, a leczenie może zapobiec
powikłaniom.
– U młodzieży z grupy ryzyka wykrywano stan
przedcukrzycowy, lecz obecnie brakuje danych
dotyczących skutecznych interwencji innych
niż takie, które i tak by zalecono nastolatkom z grupy ryzyka (zmniejszenie masy ciała, ćwiczenia
fizyczne, modyfikacja diety).
– U młodzieży, u której stwierdza się stan przedcukrzycowy,
wykrywa się nadciśnienie tętnicze,
dyslipidemię i mikroalbuminurię. Jednak zaburzenia
te obserwowano również u otyłych nastolatków
niechorujących na cukrzycę. Przemawia
to zatem za monitorowaniem i odpowiednim leczeniem
nadciśnienia tętniczego, dyslipidemii i mikroalbuminurii u młodzieży z grupy ryzyka, a nie identyfikacją nieprawidłowej glikemii.
• Dostępny jest czuły test (mało wyników fałszywie
ujemnych), charakteryzujący się także
odpowiednią swoistością (minimalna liczba
wyników fałszywie dodatnich).
– Żaden z aktualnie dostępnych testów (oznaczenie
glikemii na czczo, przygodnie, 2 h po obciążeniu
glukozą, odsetek HbA1c) nie jest wystarczająco
czuły ani swoisty, biorąc pod uwagę
rzadkie występowanie cukrzycy typu 2, nawet w populacjach obarczonych dużym ryzykiem.
– Istnieje duża niepewność odnośnie do zakresu
prawidłowych wartościach oraz znaczenia nieprawidłowych
wyników wszystkich wymienionych
pomiarów glikemii.
Obecnie istnieje jeden zbiór zaleceń dotyczących
badań przesiewowych i wychwytywania przypadków
cukrzycy wydany przez ADA w 2000 roku.
Jednak zalecenia te nadal budzą wątpliwości. Dostępne
dane wskazują, że badania przesiewowe w kierunku cukrzycy u nastolatków bez objawów
choroby wykrywają małą liczbę przypadków oraz
że konieczne są dalsze badania mające na celu
opracowanie optymalnej strategii przesiewu, ustalające
m.in. częstość wykonywania badań. Aktualnie
najlepszej jakości dane sugerują, że prowadzenie
przesiewu w kierunku cukrzycy typu 2 poza
ośrodkami badawczymi w większości populacji
nie jest efektywne kosztowo. Jedynym wyjątkiem
może być oznaczanie glukozy w moczu u młodzieży
japońskiej.
Konflikt interesów: Autorzy nie zgłosili konfliktu intetresów.
Piśmiennictwo:
1. Rosenbloom A.L., Young R.S., Joe J.R., Winter W.: Emerging epidemic of type 2 diabetes in youth. Diabetes Care, 1999; 22: 345–3542. American Diabetes Association: Type 2 diabetes in children and adolescents: consensus conference report. Diabetes Care, 2000; 23: 381–389
3. Duncan G.E.: Prevalence of diabetes and impaired fasting glucose levels among US adolescents: National Health and Nutrition Examination Survey. Arch. Pediatr. Adolesc. Med., 1999–2002; 2006; 523–528
4. Pinhas-Hamiel O., Zeitler P.: The global spread of type 2 diabetes mellitus in children and adolescents. J. Pediatr., 2005; 146: 693–700
5. Drake A.J., Smith A., Betts P.R., Crowne E.C., Sheild J.P.: Type 2 diabetes in obese white children. Arch. Dis. Child., 2002; 86: 207–208
6. Kitagawa T., Owada M., Urakami T., Yamauchi K.: Increased incidence of non-insulin dependent diabetes mellitus among Japanese school children correlates with an increased intake of animal protein and fat. Clin. Pediatr. (Phila), 1998; 37: 111–115
7. Ehtisham S., Hattersley A.T., Dunger D.B., Barrett T.G., Group BSfPEaDCT: First UK survey of paediatric type 2 diabetes and MODY. Arch. Dis. Child., 2004; 89: 526–529
8. The SEARCH for Diabetes in Youth Study Group: Incidence of diabetes in youth in the United States. JAMA, 2007; 297: 2716–2724
9. Kadiki O.A., Reddy M.R., Marzouk A.A.: Incidence of insulin-dependent diabetes (IDDM) and non-insulindependent diabetes (NIDDM) (0–34 years at onset) in Benghazi, Libya. Diabetes Res. Clin. Pract., 1996; 32: 165–173
10. Chan J.C., Cheung C.K., Swaminathan R., Nicholls M.G., Cockram C.S.: Obesity albuminuria, and hypertension among Hong Kong Chinese with non-insulin dependent diabetes mellitus (NIDDM). Postgrad. Med. J., 1993; 69: 204–210
11. Wei J.N., Sung F.C., Li C.Y., et al.: Low birth weight and high birth weight in infants are both an increased risk to have type 2 diabetes among schoolchildren in Taiwan. Diabetes Care, 2003; 26: 343–348
12. Ramachandran A., Snehalatha C., Satyavani K., Sivasankari S., Vijay V.: Type 2 diabetes in Asian-Indian urban children. Diabetes Care, 2003; 2003; 1022–1023
13. Sayeed M.A., Hunsain M.Z., Banu A., Mak R., Azad Khan A.K.: Prevalence of diabetes in a suburban population of Bangladesh. Diabetes Res. Clin. Pract., 1997; 34: 149–155
14. Braun B., Zimmerman M.B., Kretchmer N., Spargo R.M., Smith R.M., Gracey M.: Risk factors for diabetes and cardiovascular disease in young Australian aborigines: a 5-year follow-up study. Diabetes Care, 1996; 19: 472–479
15. McGrath N.M., Parker G.N., Dawson P.: Early presensation of type 2 diabetes mellitus in young New Zealand Maori. Diabetes Res. Clin. Pract., 1999; 43: 205–209
16. Eppens M.C., Craig M.E., Jones T.W., et al.: Type 2 diabetes in youth from the Western Pacific region: glycemic control, diabetes care and complications. Curr. Med. Res. Opin., 2006; 22: 1013–1020
17. Sugihara S., Sasaki N., Kohno H., et al.: Survey of current medical treatments for childhood-onset type 2 diabetes mellitus in Japan. Clin. Pediatr. Endocrinol., 2005; 14: 65–75
18. Rosenbloom A.L., Silverstein J.H., Amemiya S., Zeitler P., Klingensmith G.J.: Type 2 diabetes in children and adolescents. Pediatr. Diabetes, 2009; 10 (Suppl. 12): 17–32
19. Druet C., Tubiana-Rufi N., Chevenne D., Rigal O., Polak M., Levy-Marchal C.: Characterization of insulin secretion and resistance in type 2 diabetes of adolescents. J. Clin. Endocrinol. Metab., 2006; 91: 401–404
20. Miller J., Silverstein J.H., Rosenbloom A.L.: Type 2 diabetes in the child and adolescent. In: Lifshitz F (ed) Pediartric Endocrinology: fifth edition, volume 1. New York, Marcel Dekker, 2007; 169–188
21. United Kingdom Prospective Diabetes Study Group: Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet, 1998; 352: 837–853
22. TODAY Study Group, Zeitler P., Hirst K., et al.: A clinical trial tomaintain glycemic control in youth with type 2 diabetes. N. Engl. J. Med., 2012; 366: 2247–2256
23. TODAY Study Group: Rapid rise in hypertension and nephropathy in youth with type 2 diabetes: the TODAY clinical trial. Diabetes Care, 2013; 36: 1735–1741
24. Plourde G.: Impact of obesity on glucose and lipid profiles in adolescents at different age groups in relation to adulthood. BMC Fam. Pract., 2002; 3: 18
25. American Diabetes Association. Standards of medical care in diabetes – 2014. Diabetes Care, 2014; 37 (Suppl. 1): S14–S80
26. Libman I.M., Barinas-Michell E., Bartucci A., Robertson R., Arslanian S.: Reproducibility of the oral glucose tolerance test in overweight children. J. Clin. Endocrinol. Metab., 2008; 93: 4231–4237
27. Kapadia C.R.: Are the ADA hemoglobin A1c criteria relevant for the diagnosis of type 2 diabetes in youth? Curr. Diab. Rep., 2013; 13: 51–55
28. Umpaichitra V., Banerji M.A., Castells S.: Autoantibodies in children with type 2 diabetes mellitus. J. Pediatr. Endocrinol. Metab., 2002; 15: 525–530
29. Reinhard T., Schober E., Weigand S., Thon A., Holl R., Group obotD-WS: ß-cell autoantibodies in children with type 2 diabetes mellitus: subgroup or misclassification? Arch. Dis. Child., 2006; 91: 473–477
30. Landin-Olsson M.: Latent autoimmune diabetes in adults. Ann. NY Acad. Sci., 2002; 958: 112–116
31. Winter W.E., Maclaren N.K., Riley W.J., Clarke D.W., Kappy M.S., Spillar R.P.: Maturity onset diabetes of youth in black Americans. N. Engl. J. Med., 1987; 316: 112–116
32. Klingensmith G.J., Laffel L., Pyle L., et al.: The presence of GAD and IA-2 antibodies in youth with a type 2 diabetes phenotype. Diabetes Care, 2010; 33: 1970–1975
33. Turner R., Stratton I., Horton V., et al.: UKPDS 25: autoantibodies to islet cell cytoplasm and glutamic acid decarboxylase for pre-diction of insulin requirement in type 2 diabetes. Lancet, 1997; 350: 1288–1293
34. Laffel L., Chang N., Grey M., et al.: Metformin monotherapy in youth with recent onset type 2 diabetes: experience from the prerandomization run-in phase of the TODAY study. Pediatr. Diabetes, 2012; 13: 369–375
35. Copeland K.C., Zeitler P., Geffner M., et al.: Characteristics of adolescents and youth with recentonset type 2 diabetes: the TODAY cohort at baseline. J. Clin. Endocrinol. Metab., 2011; 96: 159–167
36. The Epidemiology of Diabetes Interventions and Complications Study Group: Sustained effect of intensive treatment of type 1 diabetes mellitus on development and progression of diabetic nephropathy: the Epidemiology of Diabetes Interventions and Complications (EDIC) study. JAMA, 2003; 290: 2159–2167
37. Urakami T., Kuwabara R., Habu M., et al.: Clinical characteristics of non-obese children with type 2 diabetes mellitus without involvement of ß-cell autoimmunity. Diabetes Res. Clin. Pract., 2013; 99: 105–111
38. Rosenbloom A.L.: Obesity, insulin resistance, beta cell autoimmunity, and the changing clinical epidemiology of childhood diabetes. Diabetes Care, 2003; 26: 2954–2956
39. Zeitler P., Haqq A., Rosenbloom A., Glaser N., Lawson Wilkins Pediatric Endocrine Society: Hyperglycemic hyperosmolar syndrome in children: pathophysiological considerations and suggested guidelines for treatment. J. Pediatr., 2011; 158: 9–14
40. Nadeau K.J., Regensteiner J.G., Bauer T.A., et al.: Insulin resistance in adolescents with type 1 diabetes and its relationship to cardiovascular function. J. Clin. Endocrinol. Metab., 2010; 95: 513–521
41. Nadeau K.J., Zeitler P.S., Bauer T.A., et al.: Insulin resistance in adolescents with type 2 diabetes is associated with impaired exercise capacity. J. Clin. Endocrinol. Metab., 2009; 94: 3682–3685
42. Cali A.M.C., Bonadonna R.C., Trombetta M., Weiss R., Caprio S.: Metabolic abnormalities underlying the different prediabetic phenotypes in obese adolescents. J. Clin. Endocrinol. Metab., 2008; 93: 1767–1773
43. Weiss R., Taksali S.E., Tamborlane W.V., Burgert T.S., Savoye M., Caprio S.: Predictors of changes in glucose tolerance status in obese youth. Diabetes Care, 2005; 28: 902–909
44. Group T.S.: Retinopathy in youth with type 2 diabetes participating in the TODAY clinical trial. Diabetes Care, 2013; 36: 1772–1774
45. Group TS: Lipid and inflammatory cardiovascular risk worsens over 3 years in youth with type 2 diabetes. Diabetes Care, 2013; 36: 1758–1764
46. Aslander-van Vliet E., Smart C., Waldron S.: Nutritional management in childhood and adolescent diabetes. Pediatr. Diabetes, 2007; 8: 323–339
47. Copeland K.C., Silverstein J., Moore K.R., et al.: Management of newly diagnosed type 2 Diabetes Mellitus (T2DM) in children and adolescents. Pediatrics, 2013; 131: e648–e664
48. Schellenberg E.S., Dryden D.M., Vandermeer B., Ha C., Korownyk C.: Lifestyle interventions for patients with and at risk for type 2 diabetes: a systematic review and meta-analysis. Ann. Intern. Med., 2013; 159: 543–551
49. Yoon U., Kwok L.L., Magkidis A.: Efficacy of lifestyle interventions in reducing diabetes incidence in patients with impaired glucose tolerance: a systematic review of randomized controlled trials. Metabolism, 2013; 62: 303–314
50. Lee S., Kim Y.: Effects of exercise alone on insulin sensitivity and glucose tolerance in obese youth. Diabetes Metab. J., 2013; 37: 225–232
51. Barlow S.E., Committee E.: Expert committee recommendations regarding the prevention, assessment, and treatment of child and adolescent overweight and obesity: summary report. Pediatrics, 2007; 120 (Suppl. 4): S164–S192
52. Fitch C., Keim K.S., Academy of Nutrition and Dietetics: Position of the academy of nutrition and dietetics: use of nutritive and nonnutritive sweeteners. J. Acad. Nutr. Diet., 2012; 112: 739–758
53. Slavin J.L., Lloyd B.: Health benefits of fruits and vegetables. Adv. Nutr., 2012; 3: 506–516
54. American Diabetes A: Standards of medical care in diabetes – 2012. Diabetes Care, 2012; 35 (Suppl. 1): S11–S63
55. Dhuper S., Buddhe S., Patel S.: Managing cardiovascular risk in overweight children and adolescents. Paediatr. Drugs, 2013; 15: 181–190
56. Jensen M.D., Ryan D.H., Apovian C.M., et al.: AHA/ACC/TOS Guideline for the Management of Overweight and Obesity in Adults: A Report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines and The Obesity Society. Circulation, 2014; 63: 2985–3023
57. Chahal H., Fung C., Kuhle S., Veugelers P.J.: Availability and night-time use of electronic entertainment and communication devices are associated with short sleep duration and obesity among Canadian children. Pediatr. Obes., 2013; 8: 42–51
58. Lane A., Harrison M., Murphy N.: Screen time increases risk of overweight and obesity in active and inactive 9 year old Irish children: a cross sectional analysis. J. Phys. Act. Health, 2013 Jun 24 [Epub ahead of print]
59. Taveras E.M., McDonald J., O’Brien A., et al.: Healthy Habits, Happy Homes: methods and baseline data of a randomized controlled trial to improve household routines for obesity prevention. Prev. Med., 2012; 55: 418–426
60. Haines J., McDonald J., O’Brien A., et al.: Healthy Habits, Happy Homes: randomized trial to improve household routines for obesity prevention among preschool-aged children. JAMA Pediatr., 2013; 167: 1072–1079
61. Robinson T.M.: Reducing children’s television viewing to prevent obesity. A randomized controlled trial. JAMA, 1999; 82: 1561–1567
62. Mays D., Streisand R., Walker L.R., Prokhorov A.V., Tercyak K.P.: Cigarette smoking among adolescents with type 1 diabetes: strategies for behavioral prevention and intervention. J. Diabetes Complications, 2012; 26: 148–153
63. Group TAS: Effects of combination lipid therapy in type 2 diabetes mellitus. N. Engl. J. Med., 2010; 362: 1563–1574
64. Bretzel R.G., Number U., Landgraf W., Owens D.R., Bradley C., Linn T.: Once-daily basal insulin glargine versus thrice-daily prandial insulin lispro in people with type 2 diabetes on oral hypoglycaemic agents (APOLLO): an open randomised controlled trial. Lancet, 2008; 371: 1073–1084
65. The TODAYT Study Group: Safety and tolerability of the treatment of youth-onset type 2 diabetes. Diabetes Care, 2013; 36: 1765–1771
66. Gottschalk M., Vlajnic A., Danne T., Cara J.F.: Glimepiride versus metformin as monotherapy in pediatric patients with type 2 diabetes: a randomized, single-blind comparative study. Diabetes Care, 2007; 30: 790–794
67. Lincoff A.M., Wolski K., Nicholls S.J., Nissen S.E.: Pioglitazone and risk of cardiovascular events in patients with type 2 diabetes mellitus: a meta-analysis of randomized trials. JAMA, 2007; 298: 1180–1188
68. Singh S., Loke Y.K., Furberg C.D.: Long-term risk of cardiovascular events with rosiglitazone: a metaanalysis. JAMA, 2007; 298: 1189–1195
69. Singh R.K., Perros P., Frier B.M.: Hospital management of diabetic ketoacidosis: are clinical guidelines implemented effectively? Diabet. Med., 1997: 14: 482–486
70. Chiasson J., Josse R., Hunt J., et al.: The efficacy of acarbose in the treatment of patients with non-insulindependent diabetes mellitus. A multicenter controlled clinical trial. Ann. Intern. Med., 1994; 121: 928–935
71. Inge T.H., Zeller M.,Garcia V.F., Daniels S.R.: Surgical approach to adolescent obesity. Adolesc. Med. Clin., 2004; 15: 429–453
72. Michalsky M.P., Inge T.H., Teich S., et al.: Adolescent bariatric surgery program characteristics: The Teen Longitudinal Assessment of Bariatric Surgery (Teen-LABS) study experience. Semin. Pediatr. Surg., 2014; 23: 5–10
73. Reaven G.: The metabolic syndrome or the insulin resistance syndrome? Different names, different concepts, different goals. Endocrinol. Metab. Clin. North Am., 2004; 33: 283–303
74. Banerjee S., Raghavan S., Wasserman E.J., Lin-Der B.L., Saenger P., Dimartino-Nardi J.: Hormonal findings in African American and Caribbean Hispanic girls with premature adrenarche: implications for polycystic ovarian syndrome. Pediatrics, 1998; 102: E35
75. Ibanez L., Potau N., Marcos M.V., Dezegher F.: Exaggerated adrenarche and hyperinsulinism in adolescent girls born small for gestational age. J. Clin. Endocrinol. Metab., 1999; 84: 4739–4741
76. Dabelea D., Crume T.: Maternal environment and the transgenerational cycle of obesity and diabetes. Diabetes, 2011; 60: 1849–1855
77. Expert Panel onDetection, Evaluation, and Treatment of High Blood Cholesterol in Adults. Executive Summary of the Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). JAMA, 2001; 285: 2486–2497
78. Ford E.S., Li C.: Defining the metabolic syndrome in children and adolescents: will the real definition please stand up? J. Pediatr., 2008; 152: 160–164
79. Zimmet P., Alberti G., Kaufman F., et al.: Themetabolic syndrome in children and adolescents. Lancet, 2007; 369: 2059–2061
80. Laurson K.R., Welk G.J., Eisenmann J.C.: Diagnostic performance of BMI percentiles to identify adolescents with metabolic syndrome. Pediatrics, 2014; 133: e330–e338
81. Kirpichnikov D., Sowers J.R.: Diabetes mellitus and diabetes-associated vascular disease. Trends Endocrinol. Metab., 2001; 12: 225–230
82. Laakso M.: Lipids in type 2 diabetes. Semin. Vasc. Med., 2002; 2: 59–66
83. Goldberg I.J.: Diabetic dyslipidemia: causes and consequences. J. Clin. Endocrinol. Metab., 2001; 86: 965–971
84. Donaghue K.C., Francesco C., Trotta D., Allgrove J., Dahl-Jorgensen K.: Microvascular and macrovascular complications. Pediatr. Diabetes, 2007; 8: 163–170
85. Wabitsch M., Hauner H., Hertrampf M., et al.: Type II diabetes and impaired glucose regulation in Caucasian children and adolescents with obesity living in Germany. Int. J. Obes., 2004; 28: 307–313
86. Wiegand S., Raile K., Reinehr T., et al.: Daily insulin requirement of children and adolescents with type 1 diabetes: effect of age, gender, body mass index and mode of therapy. Eur. J. Endocrinol., 2008; 158: 543–549
87. Shalitin S., Abrahami M., Lilos P., Phillip M.: Insulin resistance and impaired glucose tolerance in obese children and adolescents referred to a tertiary care center in Israel. Int. J. Obes., 2005; 29: 571–578
88. STOPP-T2D Study Group: Presence of diabetes risk factors in a large US eighth-grade cohort. Diabetes Care, 2006; 29: 212–217
89. Goran M.I., Bergman R.N., Avila Q., et al.: Impaired glucose tolerance and reduced ß-cell function in overweight Latino children with a positive family history for type 2 diabetes. J. Clin. Endocrinol. Metab., 2004; 89: 207–212
90. Lee S., Bacha F., Gungor N., Arslanian S.A.: Waist circumference is an independent predictor of insulin resistance in black and white youths. J. Pediatr., 2006; 148: 188–194
91. Freedman D.S., Khan L.K., Dietz W.H., Srini-Vasan S.R., Berenson G.S.: Relationship of childhood obesity to coronary heart disease risk factors in adult-hood: the Bogalusa heart study. Pediatrics, 2001; 108: 712–718
92. Berenson G.S., Srini-Vasa S.R.: Cardiovascular risk factors in youth with implications for aging: the Bogalusa Heart Study. Neurobiol. Aging., 2005; 26: 303–307
93. Juonala M., Jarvisalo M.J., Maki-Torkko N., Kahonen M., Viikari J.S., Raitakari O.T.: Risk factors identified in childhood and decreased carotid artery elasticity in adulthood: the Cardiovascular Risk in Youth Finns Study. Circulation, 2005; 112: 1486–1493
94. Visser M., Bouter L.M., McQuillan G.M., Wener M.H., Harris T.B.: Low-grade systemic inflammation in overweight children. Pediatrics, 2001; 107: e13
95. Marcus M.D., Foster G.D., El Ghormli L., et al.: Shifts in BMI category and associated cardiometabolic risk: prospective results from HEALTHY study. Pediatrics, 2012; 129: e983–e991
96. Williams C.L., Hayman L.L., Daniels S.R., et al.: Cardiovascular health in childhood: A statement for health professionals from the Committee on Atherosclerosis, Hypertension, and Obesity in the Young (AHOY) of the Council on Cardiovascular Disease in the Young, American Heart Association. Circulation, 2002; 106: 143–160
97. UKPDS Study Group: Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS. BMJ, 1998; 317: 703–713
98. Eppens M.C., Craig M.E., Cusumano J., et al.: Prevalence of diabetes complications in adolescents with type 2 compared with type 1 diabetes. Diabetes Care, 2006; 29: 1300–1306
99. West N.A., Hamman R.F., Mayer-Davis E.J., et al.: Cardiovascular risk factors among youths with and without type 2 diabetes: differences and possibile mechanisms. Diabetes Care, 2009; 32: 175–180
100. Mayer-Davis E.J., Ma B., Lawson A., et al.: Cardiovascular disease risk factors in youth with type 1 and type 2 diabetes: implications of a factor analysis of clustering. Metab. Syndr. Relat. Disord., 2009; 7: 89–95
101. Wierzbicki A.S., Nimmo L., Feher M.D.,Cox A., Foxton J., Lant A.F.: Association of angiotensin-converting enzyme DD genotype with hypertension in diabetes. J. Hum. Hypertens., 1995; 9: 671–673
102. Batisky D.L.: What is the optimal first-line agent in children requiring antihypertensive medication? Curr. Hypertens. Rep., 2012; 14: 603–607
103. National High Blood Pressure Education Working Group on High Blood Pressure in Children and Adolescents: The fourth report on the diagnosis, evaluation, and treatment of high blood pressure in children and adolescents. Pediatrics, 2004; 114 (2 Suppl. 4th Report): 555–576
104. Blowey D.L.: Update on the pharmacologic treatment of hypertension in pediatrics. J. Clin. Hypertens., 2012; 14: 383–387
105. Lurbe E., Cifkova R., Cruickshank J.K., et al.: Management of high blood pressure in children and adolescents: recommendations of the European Society of Hypertension. J. Hypertens., 2009; 27: 1719–1742
106. Ettinger L.M., Freeman K., Di Martino-Nardi J.R., Flynn J.T.: Microalbuminuria and abnormal ambulatory blood pressure in adolescents with type 2 diabetes mellitus. J. Pediatr., 2005; 147: 67–73
107. Fagot-Campagna A., Knowler W.C., Pettit D.J.: Type 2 diabetes in Pima Indian children: cardiovascular risk factors at diagnosis and 10 years later. Diabetes, 1998: 47 (Suppl. 1): A155
108. Sellers E., Young G., Dean H.: Dyslipidemia and other cardiovascular risk factors in a Canadian First Nation pediatric population with type 2 diabetes mellitus. Pediatr. Diabetes, 2007; 8: 384–390
109. Dart A.B., Sellers E.A., Martens P.J., Brownell M.D., Dean H.J.: High burden of kidney disease in youth-onset type 2 diabetes. Diabetes Care, 2012; 35: 1265–1271
110. Yokohama H., Okudaira M., Otani T., et al.: High incidence of diabetic nephropathy in early-onset Japanese NIDDM patients. Diabetes Care, 1998; 21: 1080–1085
111. Yokohama H., Okudaira M., Otani T., et al.: Higher incidence of diabetic nephropathy in type 2 than in type 1 diabetes in early-onset diabetes in Japan. Kidney Int., 2000; 58: 302–311
112. Rodriguez B.L., Fujimoto W.Y., Mayer-Davis E.J., et al.: Prevalence of cardiovascular disease risk factors inU.S. children and adolescents with diabetes: the SEARCH for diabetes in youth study. Diabetes Care, 2006; 29: 1891–1896
113. Springer S.C., Silverstein J., Copeland K., et al.: Management of type 2 diabetes mellitus in children and adolescents. Pediatrics, 2013; 131: e648–e664
114. Kavey R.E., Allada V., Daniels S.R., et al.: Cardiovascular risk reduction in high-risk pediatric patients: a scientific statement from the American Heart Association Expert Panel on Population and Prevention Science; the Councils on Cardiovascular Disease in the Young, Epidemiology and Prevention, Nutrition, Physical Activity and Metabolism, High Blood Pressure Research, Cardiovascular Nursing, and the Kidney in Heart Disease; and the Interdisciplinary Working Group on Quality of Care and Outcomes Research: endorsed by the American Academy of Pediatrics. Circulation, 2006; 114: 2710–2738
115. Expert panel on integrated guidelines for cardiovascular health and risk reduction in children and adolescents, National Heart Lung and Blood Institute. Expert panel on integrated guidelines for cardiovascular health and risk reduction in children and adolescents: summary report. Pediatrics, 2011; 128 (Suppl. 5): S213–S256
116. Flint A., Arslanian S.: Treatment of type 2 diabetes in youth. Diabetes Care, 2011; 34 (Suppl. 2): S177–S183
117. Wadwa R.P., Urbina E.M., Anderson A.M., et al.: Measures of arterial stiffness in youth with type 1 and type 2 diabetes: the SEARCH for diabetes in youth study. Diabetes Care, 2010; 33: 881–886
118. Norman R.J., Dewailly D., Legro R.S., Hickey T.E.: Polycystic ovary syndrome. Lancet, 2007; 370: 685–697
119. Amini M., Horri N., Farmani M., et al.: Prevalence of polycystic ovary syndrome in reproductive-aged women with type 2 diabetes.Gynecol. Endocrinol., 2008; 24: 423–427
120. Shafiee M.N., Khan G., Ariffin R., et al.: Preventing endometrial cancer risk in polycystic ovarian syndrome (PCOS) women: couldmetformin help? Gynecol. Oncol., 2014; 132: 248–253
121. Legro R.S., Arslanian S.A., Ehrmann D.A., et al.: Diagnosis and treatment of polycystic ovary syndrome: an Endocrine Society clinical practice guideline. J. Clin. Endocrinol. Metab., 2013; 98: 4565–4592
122. Dean H., Sellers E.: Steatohepatitis in children with type 2 diabetes mellitus. Diabetes, 2001; 50 (Suppl. 2): A378
123. Newfield R., Schwimmer J.: Non alcoholic steatohepatitis in children and adolescents with type 2 diabetes mellitus. Diabetes, 2003; 52 (Suppl. 1): A4 041 754
124. Nadeau K.J., Klingensmith F., Zeitler P.: Type 2 diabetes in children is frequently associated with elevated alanine aminotransferase. J. Pediatr. Gastroenterol. Nutr., 2005; 41: 94–98
125. Roberts E.A.: Non-alcoholic fatty liver disease (NAFLD) in children. Front. Biosci., 2005; 10: 2306–2318
126. Hudson O.D., Nunez M., Shaibi G.Q.: Ethnicity and elevated liver transaminases among newly diagnosed children with type 2 diabetes. BMC Pediatr., 2012; 12: 174
127. Sundaram S.S., Zeitler P., Nadeau K.: The metabolic syndrome and nonalcoholic fatty liver disease in children. Curr. Opin. Pediatr., 2009; 21: 529–535
128. Gaggini M., Morelli M., Buzzigoli E., DeFronzo R.A., Bugianesi E., Gastaldelli A.: Non-alcoholic fatty liver disease (NAFLD) and its connection with insulin resistance, dyslipidemia, atherosclerosis and coronary heart disease. Nutrients, 2013; 5: 1544–1560
129. Angulo P., Keach J.C., Batts K.P., Lindor K.D.: Independent predictors of liver fibrosis in patients with nonalcoholic steatohepatitis. Hepatology, 1999; 30: 1356–1362
130. Sinha S.K., Shaheen M., Rajavashisth T.B., Pan D., Norris K.C., Nicholas S.B.: Association of race/ethnicity, inflammation, and albuminuria in patients with diabetes and early chronic kidney disease. Diabetes Care, 2014; 37: 1060–1068
131. Kastelan S., Tomic M., Gverovic Antunica A., Salopek Rabatic J., Ljubic S.: Inflammation and pharmacological treatment in diabetic retinopathy. Mediators Inflamm., 2013; 2013:213 130. doi: 10.1155/2013/213 130
132. van Greevenbroek M.M., Schalkwijk C.G., Stehouwer C.D.: Obesity-associated low-grade inflammation in type 2 diabetes mellitus: causes and consequences. Neth. J. Med., 2013; 71: 174–187
133. Montane J., Cadavez L., Novials A.: Stress and the inflammatory process: a major cause of pancreatic cell death in type 2 diabetes. Diabetes Metab. Syndr. Obes., 2014; 7: 25–34
134. Vendrell J., Chacon M.R.: TWEAK: a new player in obesity and diabetes. Front. Immunol., 2013; 4: 488
135. Zhong J., Rao X., Braunstein Z., et al.: T cell costimulation protects obesity-induced adipose inflammation and insulin resistance. Diabetes, 2013; 63: 1289–1302
136. Lee J.: Adipose tissue macrophages in the development of obesity-induced inflammation, insulin resistance and type 2 diabetes. Arch. Pharm. Res., 2013; 36: 208–222
137. Rice T.B., Foster G.D., Sanders M.H., et al.: The relationship between obstructive sleep apnea and selfreported stroke or coronary heart disease in overweight and obese adults with type 2 diabetes mellitus. Sleep, 2012; 35: 1293–1298
138. Foster G.D., Sanders M.H., Millman R., Group SAR: Obstructive sleep apnea among obese patients with type 2 diabetes. Diabetes Care, 2009; 326: 1017–1019
139. Shaw J.E., Punjabi N.M., Wilding J.P., Alberti K.G., Zimmet P.Z., Prevention IDFToEa: Sleep-disordered breathing and type 2 diabetes: a report from the International Diabetes Federation Taskforce on Epidemiology and Prevention. Diabetes Res. Clin. Pract., 2008; 8: 2–12
140. Walders-Abramson N.: Depression and quality of life in youth-onset type 2 diabetes mellitus. Curr. Diab. Rep., 2014; 14: 449
141. Zenlea I.S., Mednick L., Rein J., Quinn M., Wolfsdorf J., Rhodes E.T.: Routine behavioral and mental health screening in young children with type 1 diabetes mellitus. Pediatr. Diabetes, 2013; Nov 26 [Epub ahead of print]
142. Pervanidou P., Chrousos G.P.: Metabolic consequences of stress during childhood and adolescence. Metabolism, 2012; 61: 611–619
143. Anderson B.J., Edelstein S., Abramson N.W., et al.: Depressive symptoms and quality of life in adolescents with type 2 diabetes: baseline data from the TODAY study. Diabetes Care, 2011; 34: 2205–2207
144. Lawrence J.M., Standiford D.A., Loots B., et al.: Prevalence and correlates of depressed mood among youth with diabetes: the SEARCH for diabetes in youth study. Pediatrics, 2006; 117: 1348–1358
145. Dietz W.H., Gross W.L., Kirkpatrick J.A.: Blount disease (tibia vara): another skeletal disorder associated with childhood obesity. J. Pediatr., 1982; 101: 735–737
146. Loder R.T., Aronson D.D., Greenfield M.L.: The epidemiology of bilateral slipped capital femoral epiphysis. A study of children in Michigan. J. Bone Joint Surg. Am., 1993; 75: 1141–1147
147. Constantino M.I., Molyneaux L., Limacher-Gisler F., et al.: Long-term complications and mortality in youngonset diabetes: type 2 diabetes is more hazardous and lethal than type 1 diabetes. Diabetes Care, 2013; 36: 3863–3869
148. Rhodes E.T., Prosser L.A., Hoerger T.J., Ludwig D.S., Laffel L.M.: Estimated morbidity and mortality in adolescents and young adults diagnosed with type 2 diabetes mellitus. Diabet. Med., 2012; 29: 453–463
149. Sackett D.L., Holland W.W.: Controversy in detection of disease. Lancet, 1965; ii: 357–359
















